题目内容
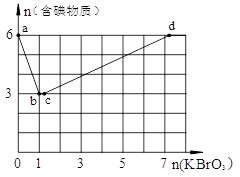
现向含6 mol KI的硫酸溶液中逐滴加入KBrO3溶液,整个过程中含碘物质的物质的量与所加入KBrO3的物质的量的关系如图所示。
请回答下列问题:
(1)b点时,KI反应完全,则消耗的氧化剂与还原剂物质的量之比为 。
(2)已知b→c过程中,仅有一种元素发生化合价变化,写出并配平该反应的离子方程式 ________________________________________。
(3)n(KBrO3) = 4时,对应含碘物质的化学式为 。

请回答下列问题:
(1)b点时,KI反应完全,则消耗的氧化剂与还原剂物质的量之比为 。
(2)已知b→c过程中,仅有一种元素发生化合价变化,写出并配平该反应的离子方程式 ________________________________________。
(3)n(KBrO3) = 4时,对应含碘物质的化学式为 。
(1)1 : 6;(2)BrO3- + 5Br- + 6H+ = 3Br2 + 3H2O(3)I2,KIO3;
试题分析:(1)b点时,KI反应完全,n(KI):n(KBrO3)=6:1,反应中KI被氧化,KBrO3被还原,反应的方程式为6I-+BrO3-+6H+=3I2+Br-+3H2O,
(2)b→c过程中,含碘物质的物质的量没有发生变化,溶液中存在Br-和BrO3-,二者发生氧化还原反应,反应的离子方程式为BrO3-+5Br-+6H+=3Br2+3H2O,
(3)n(KBrO3)=4时,溶液中含碘物质的物质的量介于3~6之间,部分I2被氧化生成KIO3,

练习册系列答案
相关题目

 CH4(g)+HC≡CH(g)+H2(g); △H1="156.6" kJ·mol-1
CH4(g)+HC≡CH(g)+H2(g); △H1="156.6" kJ·mol-1