题目内容
6.在125 mL 2mol?L-1的NaOH溶液中含有溶质10g;配制450mL 0.5mol?L-1的CuSO4溶液,需要称取CuSO4固体40 g.分析 根据n=$\frac{m}{M}$计算NaOH物质的量,再根据V=$\frac{n}{c}$计算溶液体积;
没有450mL容量瓶,应选择500mL容量瓶,配制溶液体积为500mL,根据n=cV计算CuSO4的物质的量,再根据m=nM计算CuSO4的质量.
解答 解:10g NaOH物质的量为$\frac{10g}{40g/mol}$=0.25mol,则溶液体积为$\frac{0.25mol}{2mol/L}$=0.125L=125mL,
没有450mL容量瓶,应选择500mL容量瓶,配制溶液体积为500mL,CuSO4的物质的量为0.5L×0.5mol=0.25mol,则CuSO4的质量为0.25mol×160g/mol=40g,
故答案为:125;40.
点评 本题考查物质的量有关计算、一定物质的量浓度溶液配制,注意中学常用容量瓶规格.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
16.氨基钠和氢化钠与水反应的化学反应如下:①NaNH2+H2O═NaOH+NH3↑②NaH+H2O═NaOH+H2↑,下列叙述正确的是( )
| A. | 氨基钠和氢化钠与盐酸反应都只生成一种盐 | |
| B. | 方程式②中,每生成1mol H2转移1 mol电子 | |
| C. | 氨基钠和氢化钠的晶体中都只含离子键 | |
| D. | 方程式①中,氨基钠是还原剂 |
17.某元素M的单质1.8g在过量的O2中充分燃烧,得到M2O33.4g,已知M原子核外电子数比核内中子数少1.该元素在周期表中的位置( )
| A. | 第2周期ⅢA族 | B. | 第2周期ⅥA族 | C. | 第3周期ⅤA族 | D. | 第3周期ⅢA族 |
14.铅笔芯的主要成分是石墨和黏土,这些物质按照不同的比例加以混和、压制,就可以制成铅笔芯.用铅笔写一个字消耗石墨的质量约为5×10-4克.那么一个铅笔字含有的碳原子数约为( )
| A. | 2.5×1022个 | B. | 2.5×1019个 | C. | 5×1022个 | D. | 5×1019个 |
11.下列有关实验的选项正确的是( )


| A. | 装置Ⅰ:观察Fe(OH)2的生成 | B. | 装置Ⅱ:除去Cl2中的HCl | ||
| C. | 装置Ⅲ:除去CCl4中的Br2 | D. | 装置Ⅳ:加热分解NaHCO3固体 |
18.下列有关氧化还原反应的叙述中,正确的是( )
| A. | 一定有元素化合价的升降 | B. | 没有氧参加 | ||
| C. | 氧化反应先于还原反应 | D. | 属于复分解反应 |
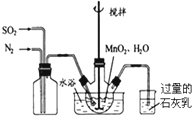 高纯MnCO3是制备高性能磁性材料的主要原料.实验室以MnO2为原料制备少量高纯MnCO3的操作步骤如下:
高纯MnCO3是制备高性能磁性材料的主要原料.实验室以MnO2为原料制备少量高纯MnCO3的操作步骤如下: