题目内容
【题目】二氧化氯(ClO2)是一种黄绿色易溶于水的气体,常用作饮用水消毒。实验室通过如下过程制备二氧化氯。
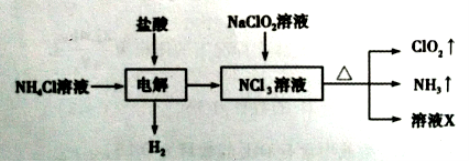
下列说法正确的是( )
A.电解时发生反应的离子方程式为NH4++3Cl-![]() 2H2↑+NCl3
2H2↑+NCl3
B.溶液X中大量存在的阴离子有Cl-、OH-
C.可用饱和食盐水除去ClO2中的NH3
D.可用明矾除去饮用水中残留的NaClO2
【答案】B
【解析】
试题分析:A、电解氯化铵与盐酸混合溶液,生成NCl3与H2,离子方程式为NH4++2H++3Cl-![]() 3H2↑+NCl3,A错误;B、根据元素守恒,溶液X中大量存在的阴离子有Cl-、OH-,B正确;C、ClO2 易溶于水,NH3 显碱性,因此要除去混有的氨气,应该选择浓硫酸,C错误;D、明矾在水中会生成氢氧化铝胶体,吸附水中的杂质起到净水的作用,但并不能除去NaClO2,D错误。答案选B。
3H2↑+NCl3,A错误;B、根据元素守恒,溶液X中大量存在的阴离子有Cl-、OH-,B正确;C、ClO2 易溶于水,NH3 显碱性,因此要除去混有的氨气,应该选择浓硫酸,C错误;D、明矾在水中会生成氢氧化铝胶体,吸附水中的杂质起到净水的作用,但并不能除去NaClO2,D错误。答案选B。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】【2016届唐山二模】亚硝酸钠是一种工业盐,外观与食盐非常相似,毒性较强。某化学兴趣小组对食盐与亚硝酸钠进行多角度探究:
(一)鉴别NaCl和NaNO2
甲同学用沉淀分析法
经查:常温下Ksp(AgNO2)=2×10-8, Ksp(AgCl)=1.8×10-10.分别向盛有5mL 0.0001 mol/L两种盐溶液的试合中同时逐滴滴加0.0001mol/L硝酸银溶液,先生成沉淀的是装有 溶液的试管。
乙同学侧定溶液pH
用pH试纸分别测定0.1 mol/L两种盐溶液的pH,测得NaNO2溶液呈碱性。该溶液呈碱性的原因是 (用离子方程式解释)。
(二)该小组用如下装置(略去夹持仪器)制备亚硝酸钠

已知:① 2NO+ Na2O2 = 2NaNO2 ;
② 酸性条件下,NO和NO2都能与MnO4一反应生成NO3一和Mn2+·
(1)使用铜丝的优点是 。
(2)装置A中反应方程式为 。
装置C 中盛放的药品是 ;(填字母代号)
A.浓硫酸 B.NaOH 溶液 C.水 D.四氯化碳
仪器F的作用 。
(3)该小组称取5.000g制取的样品溶于水配成250.0 mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol/L酸性KMnO4溶液进行滴定,实验所得数据如下表所示:
滴定次数 | 1 | 2 | 3 | 4 |
消耗KMnO4溶液体积/mL | 20.70 | 20.12 | 20.00 | 19.88 |
① 第一次实验数据出现异常,造成这种异常的原因可能是 (填字母代号)。
A.锥形瓶洗净后未干燥
B.酸式滴定管用蒸馏水洗净后未用标准液润洗
C.滴定终点时仰视读数
②酸性KMnO4溶液滴定亚硝酸钠溶液的离子方程式为 。
③该样品中亚硝酸钠的质量分数为 。


