题目内容
【题目】在10L密闭容器中,1molA和3molB在一定条件下反应:A(g)+xB(g)![]() 2C(g),2min后反应达到平衡时,测得混合气体共3.4mol,生成0.4molC,则下列计算结果不正确的是( )
2C(g),2min后反应达到平衡时,测得混合气体共3.4mol,生成0.4molC,则下列计算结果不正确的是( )
A.平衡时,物质的量比A:B:C=2:11:4
B.x值等于4
C.A的转化率20%
D.B的平均反应速率为0.04mol·L-1·min-1
【答案】A
【解析】

混合气体共3.4mol=0.8mol+(3-0.2x)mol+0.4mol,解得x=4。
A.根据方程式知,生成0.4molC需要0.2molA、0.8molB,平衡时,A、B、C的物质的量分别为(1-0.2)mol=0.8mol、(3-0.8)mol=2.2mol、0.4mol,A、B、C的物质的量之比=0.8mol:2.2mol:0.4mol=2:11:1,故A错误;
B.根据计算可知x=4,故B正确;
C.A的转化率=![]() ×100%=20%,故C正确;
×100%=20%,故C正确;
D.平衡时B的平均反应速率=![]() =0.04moL·L-1·min-1,故D正确;
=0.04moL·L-1·min-1,故D正确;
故选A。

练习册系列答案
相关题目
【题目】利用图示装置进行实验,反应进行足够长时间后装置II中实验现象正确的是
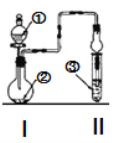
① | ② | ③ | II中实验现象 | |
A | 浓盐酸 | 大理石 | 氯化钡溶液 | 产生大量白色沉淀 |
B | 浓氨水 | 碱石灰 | 硫酸亚铁溶液 | 产生大量白色沉淀 |
C | 冰醋酸 | 乙醇和浓硫酸 | 饱和碳酸钠溶液 | 溶液分层,上层为油状液体 |
D | 浓盐酸 | KMnO4 | 氢硫酸 | 产生淡黄色沉淀 |
A.AB.BC.CD.D