题目内容
【题目】铁氮化合物(FexNy)在磁记录材料领域有着广泛的应用前景。某FexNy的制备需铁、氮气、丙酮和乙醇参与。
(1)Fe3+基态核外电子排布式为___未成对电子数为___个。
(2)丙酮(![]() )分子中碳原子轨道的杂化类型是___,丙酮分子中含有σ键的数目为____个。
)分子中碳原子轨道的杂化类型是___,丙酮分子中含有σ键的数目为____个。
(3)C、H、O三种元素的电负性由小到大的顺序为___。
(4)乙醇的沸点高于丙酮,这是因为___。
(5)利用价层电子对互斥理论判断PCl3的立体构型是___。
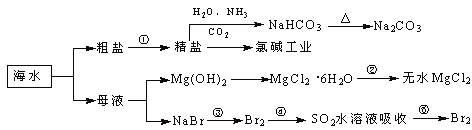
(6)某FexNy的晶胞如图-1所示,Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu替代型产物Fe(x-n) CunNy。FexNy转化为两种Cu替代型产物的能量变化如图-2 所示,其中更活泼的Cu替代型产物的化学式为___。

【答案】[Ar]3d5或1s22s22p63s23p63d5 5 sp2和sp3 9 H<C<O 乙醇分子间存在氢键 三角锥形 FeCu3N
【解析】
(1)Fe的原子序数为26,根据核外电子的排布规则书写电子排布式;
(2)![]() 中单键均为σ键,双键中含1个σ键,甲基上C形成4个σ键,C=O中C形成3个σ键,据此分析解答;
中单键均为σ键,双键中含1个σ键,甲基上C形成4个σ键,C=O中C形成3个σ键,据此分析解答;
(3)根据非金属性越强,电负性越大分析判断;
(4)乙醇分子之间形成氢键,导致沸点较高;
(5)根据价层电子对个数=σ键个数+孤电子对个数=σ键个数+![]() (a-xb)分析判断;
(a-xb)分析判断;
(6)由图2可知,Cu替代b位置的Fe时能量较高,不稳定,结合分摊法分析解答。
(1)Fe的原子序数为26,Fe3+基态核外电子数为23,3d为半满稳定结构,Fe3+基态核外电子排布式为[Ar]3d5或1s22s22p63s23p63d5,未成对电子数为5个,故答案为:[Ar]3d5或1s22s22p63s23p63d5;5;
(2)![]() 中单键均为σ键,双键中含1个σ键,1个π键,丙酮分子共有9个σ键;甲基上C形成4个σ键,C=O中C形成3个σ键,含有1个孤电子对,则羰基上C为sp2杂化,甲基上C为sp3杂化,故答案为:sp2和sp3;9;
中单键均为σ键,双键中含1个σ键,1个π键,丙酮分子共有9个σ键;甲基上C形成4个σ键,C=O中C形成3个σ键,含有1个孤电子对,则羰基上C为sp2杂化,甲基上C为sp3杂化,故答案为:sp2和sp3;9;
(3)非金属性越强,电负性越大,则C、H、O三种元素的电负性由小到大的顺序为H<C<O,故答案为:H<C<O;
(4)乙醇分子间存在氢键,而丙酮中不存在氢键,导致乙醇的沸点高于丙酮,故答案为:乙醇分子间存在氢键;
(5)PCl3中P原子的价层电子对数=3+![]() =4,P原子采用sp3杂化,含有1个孤电子对,PCl3的立体构型是三角锥形,故答案为:三角锥形;
=4,P原子采用sp3杂化,含有1个孤电子对,PCl3的立体构型是三角锥形,故答案为:三角锥形;
(6)由图2可知,Cu替代a位置的Fe时能量较低,更稳定,替代b位置的Fe时能量较高,不稳定,因此更活泼的Cu替代型产物是替代b位置的Fe,则Cu位于面心,N(Cu)=6×![]() =3,Fe位于顶点,N(Fe)=8×
=3,Fe位于顶点,N(Fe)=8×![]() =1,N位于体心,则只有1个N,其化学式为FeCu3N,故答案为:FeCu3N。
=1,N位于体心,则只有1个N,其化学式为FeCu3N,故答案为:FeCu3N。

 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案【题目】下表是元素周期表的一部分,用元素符号或化学式填空回答以下问题:
主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ⑨ | ⑩ |
⑴在这些元素中,最活泼的非金属元素是___________,化学性质最不活泼的元素是______________。
⑵表中金属性最强的元素是_______________,其原子结构示意图为 _______________________ 。
⑶表中元素的最高价氧化物对应的水化物中酸性最强的是__________,呈两性的氢氧化物是______。
⑷元素⑩的元素符号为 ____________ ,元素⑦的原序数为_________。
⑸在①~③元素中,原子半径最大的是_____________,原子半径最小的是_____________。
⑹十种元素中有一种元素的氢化物水溶液呈碱性,该氢化物的电子式为________。