题目内容
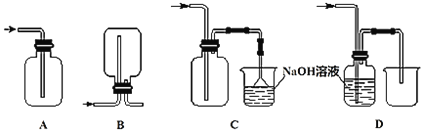
【题目】无水氯化铁加热易升华,遇潮湿空气易变质。在实验室中,可以采用如下装置和药品制取较纯的无水氯化铁固体。
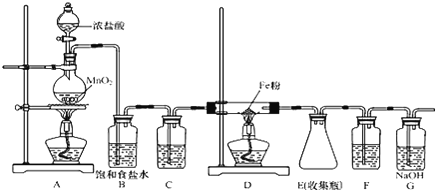
(1)制取氯化铁时,应先点燃_____(填“A”或“D”)处的酒精灯,制取氯化铁的化学方程式为_____。
(2)C、F装置中所装试剂相同,试剂均为________。
(3)下列收集Cl2的正确装置是______。
(4)G装置中反应的离子方程式为________________________________。
(5)反应后装置D中残余的固体混合物溶于稀盐酸,滴加几滴KSCN溶液。若溶液变血红色,推断固体物质的成分为______(选填序号,下同);写出溶液变血红色的离子方程式:_____________,若溶液未变血红色,推断固体物质的成分为______。
A.只有 FeCl3 B.只有Fe C.一定有FeCl3 D.一定有Fe
【答案】A ![]() 浓硫酸 C Cl2+ 2OH-= Cl-+ ClO-+ H2O C Fe3++3SCN-= Fe (SCN)3 D
浓硫酸 C Cl2+ 2OH-= Cl-+ ClO-+ H2O C Fe3++3SCN-= Fe (SCN)3 D
【解析】
⑴为排尽装置中的氧气,实验开始时,先点燃A处的酒精灯,反应生成的氯气充满D装置后再加热D处的酒精灯,铁与氯气反应![]() ,故答案为:A,
,故答案为:A,![]() ;
;
⑵C、F装置为了防止水蒸气进入E中,加入的干燥剂应为浓硫酸,故答案为:浓硫酸;
⑶A.收集气体时,集气瓶不能用橡胶塞堵住,应用双孔橡胶塞,故A错误;
B.该装置收集的是密度小于空气的气体,而氯气密度大于空气,且氯气有毒不能直接排放,故B错误;
C.该装置收集比空气密度大的气体氯气,剩余的氯气有毒需要用氢氧化钠溶液吸收,为防止倒吸,用倒扣在水面的漏斗,符合要求,故C正确;
D.氯气与氢氧化钠反应,得不到氯气,故D错误;
故答案为:C;
⑷G中氢氧化钠溶液吸收多余氯气,发生的反应为![]() ,离子方程式为
,离子方程式为![]() ,故答案为:
,故答案为:![]() ;
;
⑸滴加几滴KSCN溶液,溶液变血红色,说明溶液中有![]() ,即含有
,即含有![]() ,
,![]() 与
与![]() 反应的离子方程式
反应的离子方程式![]() ,若溶液未变血红色,说明铁粉未完全反应,铁把铁离子还原为亚铁离子。故答案为:C,
,若溶液未变血红色,说明铁粉未完全反应,铁把铁离子还原为亚铁离子。故答案为:C,![]() ,D。
,D。

 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案【题目】实验小组制备NaNO2,并探究其性质。
I.制备NaNO2
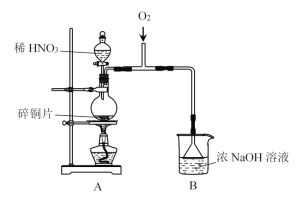
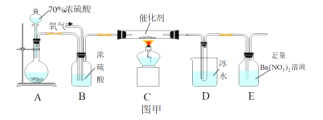
(1)A中发生反应的化学方程式是__________。
(2)B中选用漏斗替代长直导管的优点是________。
(3)为检验B中制得NaNO2,甲进行以下实验:
序号 | 试管 | 操作 | 现象 |
① | 2 mLB中溶液 | 加2 mL 0.1 mol/LKI溶液,滴加几滴淀粉溶液 | 不变蓝 |
② | 2 mLB中溶液 | 滴加几滴H2SO4至pH=5,加2 mL 0.1 mol/LKI溶液,滴加几滴淀粉溶液 | 变蓝 |
③ | 2 mLH2O | 滴加几滴H2SO4至pH=5,加2 mL 0.1 mol/LKI溶液,滴加几滴淀粉溶液 | 不变蓝 |
实验③的目的是________。
(4)乙认为上述3组实验无法证明B中一定含NaNO2,还需补充实验,理由是_________。
II.探究NaNO2的性质
装置 | 操作 | 现象 |
| 取10 mL1 mol/LNaNO2溶液于试剂瓶中,加入几滴H2SO4酸化,再加入10 mL1 mol/LFeSO4溶液,迅速塞上橡胶塞,缓缓通入足量O2。 | i.溶液迅速变为棕色; ii.溶液逐渐变浅,有无色气泡产生,溶液上方为浅红棕色。 iii.最终形成棕褐色溶液。 |
资料:i.[Fe(NO)]2+在溶液中呈棕色。
ii.HNO2在溶液中不稳定,易分解产生NO和NO2气体。
(5)溶液迅速变为棕色的原因是_________。
(6)已知棕色溶液变浅是由于生成了Fe3+,反应的离子方程式是_________。
(7)最终棕褐色溶液的成分是Fe(OH)x(SO4)y,测得装置中混合溶液体积为20 mL,设计如下实验测定其组成。
资料:充分反应后,Fe2+全部转化为Fe(OH)x(SO4)y。
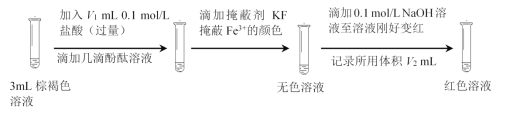
Fe(OH)x(SO4)y中x=_______(用含V1、V2的代数式表示)。
【题目】下表为短周期元素,表中所列序号分别代表一种元素。(除说明外都用化学用语填空)
① | ② | |||||||
③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
(1)上述元素中金属性最强和非金属性最强的元素名称分别是______,_______;
(2)①和②的气态氢化物稳定性比较(写化学式):______________;
(3)在上述元素中其最高价氧化物对应水化物酸性最强的酸为_________;写出⑤单质与③的最高价氧化物对应水化物反应的化学方程式为____________ 。描述H2在⑧单质中燃烧的现象___________________;
(4)现有上表中某一种元素,其单质通入到紫色石蕊溶液中的现象为先变红后褪色,该元素在周期表中的位置是_________________;
(5)比较②和③对应简单离子的离子半径大小(用相应离子符号表示)________;
(6)写出③的最高价氧化物对应水化物的电子式___________;其含有的化学键类型是____________。