��Ŀ����
����Ŀ����һ��ʵ������ͼ��װ���Ʊ�SO3���ⶨSO2������ΪSO3��ת���ʡ�
��֪��SO3�۵�Ϊ16.8�棬�е�Ϊ44.8�棬�����������װ�ÿ��Ա���ȫ���գ������ǿ�����Ӱ�졣

��1��A��ʹ��Ũ�������������Ϊ70%��ԭ����___��B��ŨH2SO4��������___��
��2����ʵ��ֹͣͨ��SO2��Ϩ��ƾ��ƺ���Ҫ����ͨһ��ʱ�����������Ŀ����___��
��3��ʵ���������װ��D������ag��װ��E�еij���ϴ�Ӻ�ɺ�������Ϊbg����E�еij����Ļ�ѧ�ɷ���___����д��ѧʽ������ʵ����SO2ת����Ϊ___���ô���ʽ��ʾ�����û���
������SO3����Ũ�����ɵõ��������ᣬ��ҵ�ϰѸ�����Ȼ�������ͨ�뵽���������п��Եõ�HSO3Cl��HSO3Cl��һ����ɫҺ�壬�е�Ϊ152�棬��ǿ��ʴ�ԣ���ʪ��������ǿ�ҵİ���������ͼ����ʾ��װ����ȡHSO3Cl���гּ�����װ����ȥ����

��1��HSO3Cl��ʪ��������ǿ�ҵİ����������û�ѧ����ʽ������ԭ��___��
��2����Һ©���·��ӵ�ëϸ�ܣ���������___��������ëϸ�ܶ�ֱ���÷�Һ©��ע��Ũ���ᣬ���ܷ�����������___��
��3��װ��F��������___��
���𰸡�����̫ϡ��SO2������ˮ������SO2�ݳ�������̫Ũ���������������Ũ�ȼ�С����Ӧ����SO2���ʱ�С �ٸ�������ڿ������٣�ʹ���������������ı���ԼΪ2��1��ʹ����������Ȼ�� �ž�������װ���е�SO2��SO3��ʹ�䱻������գ�ʹ��õĽ����ȷ BaSO4 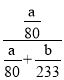 ��100% HSO3Cl+H2O=HCl+H2SO4��HCl������ʪ�������γ�����СҺ�� ����Ũ�����������ʹ�仺������Ũ������ Һ��ɽ����У� ����ʣ�������ڷ�ֹ������ˮ�ֽ���E
��100% HSO3Cl+H2O=HCl+H2SO4��HCl������ʪ�������γ�����СҺ�� ����Ũ�����������ʹ�仺������Ũ������ Һ��ɽ����У� ����ʣ�������ڷ�ֹ������ˮ�ֽ���E
��������
��һ����1����SO2���ܽ��Ժ���ȡSO2�ķ�Ӧ���ʷ��濼�ǣ�ʹ����������Ϊ70%��Ũ�������������Ʒ�Ӧ��ȡSO2��
��2����֤SO2��SO3�����ⶨȷ��
��3��װ��D���ӵ�����Ϊag��������SO3������Ϊag��װ��E�е�SO2�����ᱵ��Һ��Ӧ���ɵİ�ɫ����ΪBaSO4��������Ϊbg�����������غ㶨���Լ�ת����=![]() �����㣻
�����㣻
��������1��HSO3Cl��ʪ�����е�ˮ��Ӧ����HCl��HCl������ʪ�������γ�����СҺ�Σ�
��2����Һ©���·��ӵ�ëϸ�ܿɿ�������ļ����ٶȣ���ֹ������ڷɽ���
��3��װ��F��������β�������Լ���ֹ�����е�ˮ��������E�С�
��һ����1������̫ϡ��SO2������ˮ������SO2�ݳ�������̫Ũ���������������Ũ�ȱȽ�С����Ӧ����SO2���ʱȽ�����
��2��Ϊȷ��ʵ���ȷ�ȣ�Ҫ��֤SO2��SO3�����IJⶨȷ����ֹͣͨ��SO2��Ϩ��ƾ��ƺ���Ҫ����ͨ��һ��ʱ��O2��������װ���е�SO2��SO3��ֱ������װ�����գ�
��3��װ��D���ӵ�����Ϊag��������SO3������Ϊag��n(SO3)=![]() =
=![]() �����Է�Ӧ�б�������SO2�����ʵ���Ϊ
�����Է�Ӧ�б�������SO2�����ʵ���Ϊ![]() ��װ��E�е�SO2�����ᱵ��Һ��Ӧ����bg��ɫ����ΪBaSO4��n(BaSO4)=
��װ��E�е�SO2�����ᱵ��Һ��Ӧ����bg��ɫ����ΪBaSO4��n(BaSO4)=![]() =
=![]() ������Sԭ���غ㣬��Ӧ��ʣ��SO2�����ʵ���Ϊ
������Sԭ���غ㣬��Ӧ��ʣ��SO2�����ʵ���Ϊ![]() ������SO2��ת����Ϊ��
������SO2��ת����Ϊ��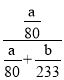 ��100% ��
��100% ��
��������1��HSO3Cl��ʪ�����е�ˮ������Ӧ������HCl��HCl������ʪ�������γ�����СҺ�Σ��γɰ�������Ӧ����ʽΪHSO3Cl+H2O=HCl+H2SO4��
��2����Һ©���·��ӵ�ëϸ�ܣ��������ǿ�������ļ���������ʹ������HCl���������ʵ��ȶ���������ëϸ�ܶ�ֱ���÷�Һ©��ע��Ũ���ᣬŨ����ϡ�ͷ��ȿ�����������ڷɽ���
��3��װ��F������������ʣ��������ֹ��Ⱦ��������ֹ������ˮ�ֽ���E��HSO3Cl��Ӧ��

 ���ƿ�����ϵ�д�
���ƿ�����ϵ�д� ���¿쳵����������ϵ�д�
���¿쳵����������ϵ�д�����Ŀ��Li4Ti5O12��LiFePO4��������ӵ�صĵ缫���ϣ���������������Ҫ�ɷ�ΪFeTiO3������������MgO��SiO2�����ʣ����Ʊ��������������£�
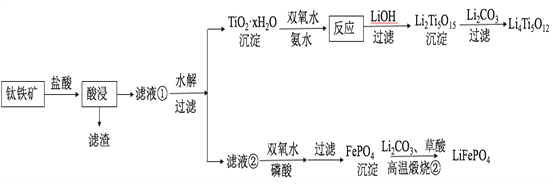
�ش��������⣺
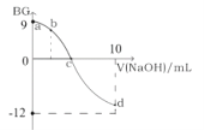
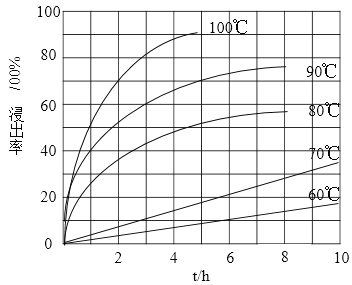
��1���������ʵ���У����Ľ����ʽ������ͼ��ʾ����ͼ��֪�������ľ�����Ϊ70%ʱ�������õ�ʵ������Ϊ___________________��
��2���������������Ҫ��TiOCl42����ʽ���ڣ�д����Ӧ��Ӧ�����ӷ���ʽ__________________��
��3��TiO2��xH2O������˫��ˮ����ˮ��Ӧ40 min����ʵ�������±���ʾ��
�¶�/�� | 30 | 35 | 40 | 45 | 50 |
TiO2��xH2Oת����% | 92 | 95 | 97 | 93 | 88 |
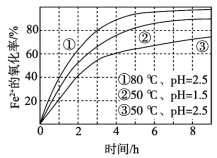
����40��ʱTiO2��xH2Oת������ߵ�ԭ��__________________��
��4��Li2Ti5O15��Ti�Ļ��ϼ�Ϊ+4�����й���������ĿΪ__________________��
��5��������Һ�ڡ���c(Mg2+)=0.02 mol/L������˫��ˮ�����ᣨ����Һ�������1������ʹFe3+ǡ�ó�����ȫ����Һ��c(Fe3+)=1��10-5 mol/L����ʱ�Ƿ���Mg3(PO4)2�������ɣ�___________����ʽ���㣩��
FePO4��Mg3(PO4)2��Ksp�ֱ�Ϊ1.3��10-22��1.0��10-24��
��6��д�����������բڡ�����FePO4�Ʊ�LiFePO4�Ļ�ѧ����ʽ______��