题目内容
【题目】从下列实验事实所引出的相应结论正确的是
选项 | 实验事实 | 结论 |
A | 其他条件相同,Na2S2O3与H2SO4反应时c(Na2S2O3)越大,析出S沉淀的时间越短 | 当其他条件不变时,增大反应物浓度,化学反应速率加快 |
B | 在化学反应前后,催化剂的质量和化学性质都没有发生改变 | 催化剂一定不参与化学反应 |
C | 物质的量浓度相同的盐酸和醋酸分别与等质量的、形状相同的锌粒反应 | 反应开始时速率相同 |
D | 在容积可变的密闭容器中发生反应H2(g)+I2(g) | 正反应速率加快,逆反应速率不变 |
A. A B. B C. C D. D
【答案】A
【解析】
A、反应物浓度增大,反应速率加快;
B、催化剂改变反应的途径,参与反应;
C、金属与反应时,氢离子浓度相同,则速率相同;
D、容积缩小一倍,压强增大
A项、其他条件相同,Na2S2O3溶液浓度越大,析出硫沉淀所需要的时间越短,是因反应物浓度增大,反应速率加快,故A正确;
B项、催化剂改变反应的途径,参与反应,但反应前后其质量和化学性质不变,故B错误;
C项、金属与反应时,氢离子浓度相同,则速率相同,物质的量浓度相同的盐酸和醋酸,盐酸中氢离子浓度大于醋酸,则反应开始时速率盐酸大于醋酸,故C错误;
D项、容积缩小一倍,压强增大,则正逆反应速率均增大,故D错误。
故选A。

【题目】氢气作为清洁能源有着广泛的应用前景,含硫天然气制备氢气的流程如下。

请回答下列问题:
I.转化脱硫:将天然气压入吸收塔,30℃时,在T.F菌作用下,酸性环境中脱硫过程示意图如下。
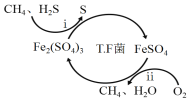
(1)过程i的离子反应方程式为_________________________________________。
(2)已知:
①Fe3+在pH=l.9时开始沉淀,pH=3.2时沉淀完全。
②30℃时,在T.F菌作用下,不同pH的FeSO4溶液中Fe2+的氧化速率如下表。
pH | 0.7 | 1.1 | 1.5 | 1.9 | 2.3 | 2.7 |
Fe2+的氧化速率/g·L-1·h-1 | 4.5 | 5.3 | 6.2 | 6.8 | 7.0 | 6.6 |
在转化脱硫中,请在上表中选择最佳pH范围是_______<pH<_______,这样选择的原因是:_______________________________________________。
Ⅱ.蒸气转化:在催化剂的作用下,水蒸气将CH4氧化。结合下图回答问题。
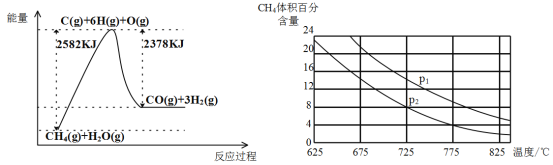
(3)①该过程的热化学方程式是__________________________________________。
②比较压强P1和p2的大小关系:P1 _________ P2(选填“>”“<”或“=”)。
③在一定温度和一定压强下的体积可变的密闭容器中充入1molCH4和1mol的水蒸气充分反应达平衡后,测得起始时混合气的密度是平衡时混合气密度的1.4倍,若此时容器的体积为2L,则该反应的平衡常数为______________(结果保留2位有效数字)。
Ⅲ.CO变换:500℃时,CO进一步与水反应生成CO2和H2。
Ⅳ.H2提纯:将CO2和H2分离得到H2的过程如示意图
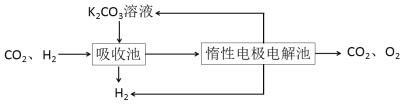
(4)吸收池中发生反应的离子方程式是____________________________________。