题目内容
【题目】短周期元素W、X、Y、Z在元素周期表中的相对位置如表所示,这四种元素的原子最外层电子数之和为21.则下列说法不正确的是
X | Y | ||
W | Z |
A.原子半径大小:![]()
B.W、Z的最高价氧化物的水化物的酸性,Z强于W
C.可用W与X的氧化物反应来制备X
D.Y与氢元素可以形成原子个数比为1:1的化合物
【答案】C
【解析】
由短周期元素W、X、Y、Z在元素周期表中的相对位置可知,X、Y位于第二周期,W、Z位于第三周期,设X的最外层电子数为x,四种元素的原子最外层电子数之和为21,则x+x+2+x+x+3=21,解得x=4,可知X为C、Y为O、W为Si、Z为Cl,然后结合元素周期律来解答。
由上述分析可知,X为C、Y为O、W为Si、Z为Cl;
A.电子层越多,原子半径越大,则原子半径大小:W>Y,故A正确;
B.非金属性越强,对应最高价含氧酸的酸性越强,则W、Z的最高价氧化物的水化物的酸性,Z强于W,故B正确;
C.W为Si、X的氧化物为CO或二氧化碳,不能反应制备X,故C错误;
D.Y与氢元素可以形成原子个数比为1:1的化合物为过氧化氢,故D正确;
故答案为C。

 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案【题目】写出下列有机物的系统命名或结构简式:
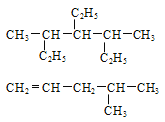
(1)_____________
(2)_____________
(3)4,4,5-三甲基-2-己炔 _______________
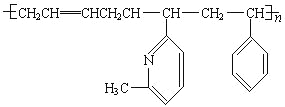
(4)新型弹性材料“丁苯吡橡胶”的结构简式如下:其单体为______________(有几种写几种)
(5)如下表所示,为提纯下列物质(括号内为少量杂质),填写所选用的除杂试剂与主要分离方法
不纯物质 | 除杂试剂 | 分离方法 | |
1 | 溴苯(Br2) | __________ | __________ |
2 | 乙醛(乙酸) | __________ | __________ |
3 | 乙酸乙酯(乙酸) | __________ | __________ |
4 | 乙醇(苯酚) | __________ | __________ |
5 | 硝基苯(硝酸) | __________ | __________ |
(6)①C5H12O的醇,在一定条件下能发生催化氧化反应,产物能与新制的氢氧化铜反应生成红色沉淀,醇的核磁共振氢谱中有三组峰,写出满足上述条件的醇的结构简式______
②C5H12O的醇,在一定条件下不能发生消去反应,写出满足条件的醇的结构简式______
③分子式为C5H12O,不能与金属钠反应.核磁共振氢谱中有四组峰,峰的面积比为3:2:1:6,写出满足上述条件的物质的结构简式______.

