题目内容
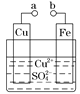
【题目】潮湿环境、Cl-、溶解氧是造成青铜器锈蚀的主要环境因素,腐蚀严重的青铜器表面大多存在起催化作用的多孔催化层。图为青铜器发生电化学腐蚀的原理示意图,下列说法正确的是( )

A.腐蚀过程中,青铜基体是正极
B.若有64gCu腐蚀,理论上耗氧体积为22.4L(标准状况)
C.多孔催化层的形成加速了青铜器的腐蚀速率,是因为改变了反应的焓变
D.环境中的Cl-、正负极产物作用生成多孔粉状锈,其离子方程式为:2Cu2++3OH-+Cl-=Cu2(OH)3Cl↓
【答案】D
【解析】
据图可知,O2得电子生成OH–,Cu失去电子生成Cu2+,过程中发生了吸氧腐蚀。据此可判断出原电池的正负极。根据原电池的工作原理,可写出电极反应式,根据得失电子守恒可进行相关计算。据此分析。
A.根据图示可知,Cu失去电子生成Cu2+,故腐蚀过程中,青铜基体是负极,A项错误;
B.由题给信息可知,原电池负极的电极反应式为:Cu-2e–=Cu2+,正极电极反应式为:O2+2H2O+4e–=4OH–,根据得失电子守恒可得关系式:2Cu~O2,据此可知,若有64gCu腐蚀,理论上耗氧体积为![]() (标准状况),B项错误;
(标准状况),B项错误;
C.多孔催化层起催化剂的作用,催化剂能降低反应的活化能,从而加快反应速率,但不能改变反应的初态和终态,所以反应焓变不变,C项错误;
D.根据题给信息,结合原电池的电极产物,可知Cl–与正负极产物发生反应:2Cu2++3OH–+Cl–=Cu2(OH)3Cl↓,D项正确;
答案选D。

【题目】根据杂化轨道理论和价层电子对互斥模型,判断下列分子或者离子的空间构型正确的是
选项 | 分子式 | 中心原子杂化方式 | 价层电子对互斥模型 | 分子或离子的立体构型 |
A | SO2 | sp | 直线形 | 直线形 |
B | HCHO | sp2 | 平面三角形 | 三角锥形 |
C | H3O+ | sp2 | 四面体形 | 平面三角形 |
D | NH4+ | sp3 | 正四面体形 | 正四面体形 |
A. AB. BC. CD. D
【题目】下表是元素周期表的一部分,按要求填空(填元素符号或化学式):
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)写出③和⑧的单质反应产物的电子式________。
(2)![]() 在周期表中的位置________,它与氧气完全燃烧的产物的电子式________;
在周期表中的位置________,它与氧气完全燃烧的产物的电子式________;
(3)在③与④的单质中,化学性质较活泼的是________,判断的实验依据是________;