题目内容
【题目】下列说法正确的是
A. 碳酸钠是重要化工原料,可用于制玻璃、造纸等
B. SO2可用于漂白纸浆、草帽和酸性高锰酸钾溶液
C. 溴单质只存在于海洋中,因此溴被称为“海洋元素”
D. 常温下铁遇浓硫酸不反应,因此可用铁槽车储运浓硫酸
【答案】A
【解析】A、碳酸钠是重要化工原料,可用于制玻璃、造纸等,选项A正确;B、SO2可用于漂白纸浆、草帽,但和酸性高锰酸钾溶液反应是发生氧化还原反应不是漂白,选项B错误;C、溴被称为“海洋元素”,但海水中不存在溴单质,选项C错误;D、常温下铁遇浓硫酸钝化而不是不反应,可用铁槽车储运浓硫酸,选项D错误。答案选A。

【题目】硫酸锌可作为食品锌强化剂的原料。工业上常用菱锌矿生产硫酸锌,菱锌矿的主要成分是ZnCO3,并含少量的Fe2O3 、FeCO3 、MgO、CaO等,生产工艺流程示意如下:
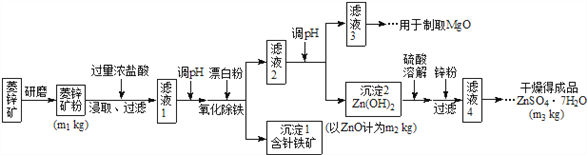
请回答下列问题:
(1)将菱锌矿研磨成粉的目的是:______________________________。
(2)漂白粉的有效成分是NaClO,请完成“氧化除铁”步骤中反应的离子方程式:_______________________
□Fe(OH)2+ □ClO- + □_____= □Fe(OH)3 + □ Cl-
(3)针铁矿(Goethite)是以德国诗人歌德(Goethe)名字命名的,组成元素是Fe、O和H,相对分子质量为89,化学式是____________(不用考虑化学式中各元素的排列顺序)。
(4)根据下表数据,调节“滤液2”的pH时,理论上可选用的最大区间为________________。
Mg(OH)2 | Zn(OH)2 | |
开始沉淀的pH | 10.4 | 6.4 |
沉淀完全的pH | 12.4 | 8.0 |
开始溶解的pH | — | 10.5 |
(5)假设各步转化均完全,分析图中数据可知:菱锌矿粉中ZnCO3的质量是_____________。