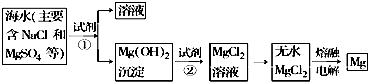
��Ŀ����
3�������й�˵����ȷ���ǣ�������| A�� | �ڢ�A��Ԫ�ض��ǵ��͵Ľ���Ԫ�� | |
| B�� | �������ڵ�Ԫ�ص�ԭ�Ӻ��ⶼ���������Ӳ� | |
| C�� | F��Cl��O��N����Ԫ�ض��ǵڢ�A���Ԫ�� | |
| D�� | ԭ�ӵ���������������ӵ�Ԫ�ض��ڵڢ�A�� |
���� A���ڢ�A��Ԫ�ذ���H�ͼ����Ԫ�أ�
B�����Ӳ���=��������
C������������=��������
D��ԭ�ӵ���������������ӵ�Ԫ�أ�����ΪHe��������������ɽ�����
��� �⣺A���ڢ�A��Ԫ�ذ���H�ͼ����Ԫ�أ�HΪ�ǽ���Ԫ�أ���A����
B������Ӳ���=����������������ڵ�Ԫ�ص�ԭ�Ӻ��ⶼ���������Ӳ㣬��B��ȷ��
C������������=��������������Ԫ�ض��ǵڢ�A���Ԫ�أ���Ϊ��A��Ԫ�أ���Ϊ��A��Ԫ�أ���C����
D��ԭ�ӵ���������������ӵ�Ԫ�أ�����ΪHe��������������ɽ�������һ���ڵڢ�A�壬��D����
��ѡB��
���� ���⿼��Ԫ�����ڱ��Ľṹ��Ӧ�ã�Ϊ��Ƶ���㣬����ԭ�ӽṹ��Ԫ��λ�õĹ�ϵΪ���Ĺؼ������ط��������Ŀ��飬ע������Ԫ�ص�λ�ã���Ŀ�ѶȲ���

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ
14��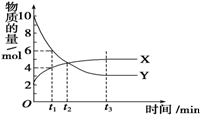 һ���¶������ܱ������ڽ�����ijһ��Ӧ��X���塢Y��������ʵ����淴Ӧʱ��仯��������ͼ��ʾ��������������ȷ���ǣ�������
һ���¶������ܱ������ڽ�����ijһ��Ӧ��X���塢Y��������ʵ����淴Ӧʱ��仯��������ͼ��ʾ��������������ȷ���ǣ�������
 һ���¶������ܱ������ڽ�����ijһ��Ӧ��X���塢Y��������ʵ����淴Ӧʱ��仯��������ͼ��ʾ��������������ȷ���ǣ�������
һ���¶������ܱ������ڽ�����ijһ��Ӧ��X���塢Y��������ʵ����淴Ӧʱ��仯��������ͼ��ʾ��������������ȷ���ǣ�������| A�� | ��Ӧ�Ļ�ѧ����ʽΪ5Y?X | B�� | t1ʱ��Y��Ũ����XŨ�ȵ�1.5�� | ||
| C�� | t2ʱ�������淴Ӧ������� | D�� | t3ʱ���淴Ӧ���ʴ�������Ӧ���� |
18����������Ԫ�صĻ�̬ԭ�ӵĵ����Ų�ʽ���£���1s22s22p63s1��1s22s22p63s23p5����1s22s22p5���������йرȽ�����ȷ���ǣ�������
| A�� | ��һ�����ܣ��ڣ��� | B�� | �縺�ԣ��ۣ��� | ||
| C�� | �����ܣ�NaCl��NaF | D�� | ��������ϼۣ��ۣ��� |
8���������ʵ�ˮ��Һ�ܵ��磬�����ڷǵ���ʵ��ǣ�������
| A�� | CH3COOH | B�� | Na2O | C�� | H2SO4 | D�� | SO2 |
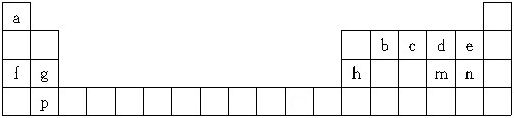
12��A��B��C��D��E��Ԫ�����ڱ���ǰ�����������ֳ���Ԫ�أ��������Ϣ���±���
��ش��������⣺
��1��E��Ԫ�����ڱ��е�λ�õ������ڵڢ��壻Dԭ�ӽṹʾ��ͼ��
��2��B��C��D�ļ����Ӱ뾶�ɴ�С��˳��Ϊ���û�ѧ���ű�ʾ����ͬ��S2-��O2-��Na+��B��D�ļ���̬�⻯�����ȶ��Խϴ����H2O
��3��B��C�ĵ��ʰ����ʵ�����1��2�γɵĻ������л�ѧ��������Ϊ���Ӽ����ü������û��������ʽΪ ��
��
��4��E��һ�־��д��Եĺ�ɫ���巢�����ȷ�Ӧ�Ļ�ѧ����ʽ��3Fe3O4+8Al$\frac{\underline{\;����\;}}{\;}$9Fe+4Al2O3��
| Ԫ�� | �����Ϣ |
| A | ԭ�Ӻ���L���������K���2�� |
| B | ��һ�ֵ��ʱ���Ϊ��������ġ�����ɡ�� |
| C | ��ɫ��Ӧ�ʻ�ɫ |
| D | ��Bͬ����Ķ�����Ԫ�� |
| E | ���γɶ������������һ��Ϊ���д��Եĺ�ɫ���� |
��1��E��Ԫ�����ڱ��е�λ�õ������ڵڢ��壻Dԭ�ӽṹʾ��ͼ��

��2��B��C��D�ļ����Ӱ뾶�ɴ�С��˳��Ϊ���û�ѧ���ű�ʾ����ͬ��S2-��O2-��Na+��B��D�ļ���̬�⻯�����ȶ��Խϴ����H2O
��3��B��C�ĵ��ʰ����ʵ�����1��2�γɵĻ������л�ѧ��������Ϊ���Ӽ����ü������û��������ʽΪ
 ��
����4��E��һ�־��д��Եĺ�ɫ���巢�����ȷ�Ӧ�Ļ�ѧ����ʽ��3Fe3O4+8Al$\frac{\underline{\;����\;}}{\;}$9Fe+4Al2O3��
13����600Kʱ����Ӧ2NO+O2�T2NO2ʵ���������£�
д����Ӧ���ʷ���ʽ�ͷ�Ӧ������
| ��ʼŨ��/��mol•L-1�� | ��ʼ����/mol•L-1s-1 | |
| c��NO�� | c��O2�� | |
| 0.010 | 0.010 | 2.5��10-3 |
| 0.010 | 0.020 | 5.0��10-1 |
| 0.030 | 0.020 | 4.5��10-2 |
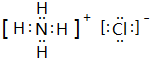 ��
��