题目内容
把0.1mol铝投入100mL 3mol/L的NaOH溶液中充分反应,再滴入120mL 1mol/L的H2SO4溶液,其结果是
( )
( )
| A、溶液的pH>7 |
| B、得到澄清透明的溶液 |
| C、得到浑浊液体 |
| D、先有沉淀生成后逐渐溶解 |
考点:铝的化学性质
专题:几种重要的金属及其化合物
分析:100mL 3mol/L的NaOH溶液中n(NaOH)=c×v=3mol/L×0.1L=0.3mol,铝投入到一定量的NaOH溶液中,发生2Al+2NaOH+2H2O=2NaAlO2+3H2↑,0.1mol铝消耗0.1mol的NaOH,生成0.1molNaAlO2,有0.2molNaOH剩余,再滴入120mL 1mol/L的H2SO4溶液,加入的硫酸的物质的量为:n(H2SO4)=c×v=1mol/L×0.12L=0.12mol,2NaOH+H2SO4=Na2SO4+2H2O,0.2molNaOH需0.1molH2SO4中和,剩余0.02molH2SO4,即0.04molH+,氢离子和偏铝酸根离子先后发生AlO2-+H++H2O=Al(OH)3↓,Al(OH)3+3H+=Al3++3H2O,因0.1molNaAlO2,需0.1mol的氢离子全部转化成氢氧化铝沉淀,显然0.04molH+,量不足,最终只有沉淀,沉淀不溶解.
解答:
解:100mL 3mol/L的NaOH溶液中n(NaOH)=c×v=3mol/L×0.1L=0.3mol,120mL 1mol/L的H2SO4溶液,n(H2SO4)=c×v=1mol/L×0.12L=0.12mol,0.1mol铝投入100mL 3mol/L的NaOH溶液中充分反应,发生2Al+2NaOH+2H2O=2NaAlO2+3H2↑,0.1mol铝消耗0.1mol的NaOH,生成0.1molNaAlO2,有0.2molNaOH剩余,再滴入0.12mol的H2SO4溶液,2NaOH+H2SO4=Na2SO4+2H2O,消耗0.1molH2SO4,剩余0.02molH2SO4,即0.04molH+,氢离子和偏铝酸根离子先后发生AlO2-+H++H2O=Al(OH)3 ↓,Al(OH)3+3H+=Al3++3H2O,因0.1molNaAlO2,需0.1mol的氢离子全部转化成氢氧化铝沉淀,显然0.04molH+,量不足,最终只有沉淀,沉淀不溶解.
A.最终生成0.04mol氢氧化铝沉淀和0.06molNaAlO2溶液,偏氯酸钠为强碱弱酸盐,溶液显碱性,故A正确;
B.最终生成0.04mol氢氧化铝沉淀,故B错误;
C.最终生成0.04mol氢氧化铝沉淀和0.06molNaAlO2溶液,得到浑浊液体,故C正确;
D.因0.1molNaAlO2,需0.1mol的氢离子全部转化成氢氧化铝沉淀,显然0.04molH+,量不足,最终只有沉淀,沉淀不溶解,故D错误;
故选AC.
A.最终生成0.04mol氢氧化铝沉淀和0.06molNaAlO2溶液,偏氯酸钠为强碱弱酸盐,溶液显碱性,故A正确;
B.最终生成0.04mol氢氧化铝沉淀,故B错误;
C.最终生成0.04mol氢氧化铝沉淀和0.06molNaAlO2溶液,得到浑浊液体,故C正确;
D.因0.1molNaAlO2,需0.1mol的氢离子全部转化成氢氧化铝沉淀,显然0.04molH+,量不足,最终只有沉淀,沉淀不溶解,故D错误;
故选AC.
点评:本题主要考查了铝及其化合物的性质,掌握铝和碱的反应,以及偏铝酸盐和酸的反应时解答的关键,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
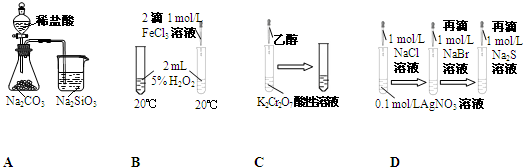
下图所示的实验装置或操作合理的是( )
A、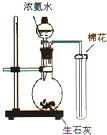 制氨气 |
B、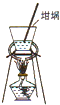 蒸发、结晶 |
C、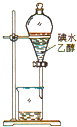 萃取碘 |
D、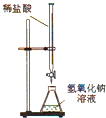 酸碱中和滴定 |
下列离子方程式书写正确的是( )
| A、偏铝酸钠中通足量的CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
| B、氯化铝溶液与足量氨水反应:Al3++4OH-═AlO2-+2H2O |
| C、氯化铝溶液与足量NaOH溶液反应:Al3++3OH-═Al(OH)3↓ |
| D、氧化铝和适量的烧碱溶液反应:Al2O3+2OH-═2AlO2-+H2O |
下列有关说法不正确的是( )
| A、互为同系物的有机物其组成元素相同,且结构必须相似 |
| B、分子组成相差一个或若干个CH2原子团的化合物一定互为同系物 |
| C、分子式为C3H6与C6H12的两种有机物一定互为同系物 |
| D、互为同系物的有机物其相对分子质量数值一定相差14n(n为正整数) |
下列离子方程式正确的是( )
| A、氧化铁溶于氢碘酸:Fe2O3+6H+═2Fe3++3H2O | ||||
| B、在AgCl沉淀中加入碘化钾溶液:AgCl(s)+I-(aq)═AgI (s)+Cl-(aq) | ||||
C、铜与浓硫酸共热:Cu+4H++SO42-
| ||||
D、电解氯化镁溶液:2Cl-+2H2O
|
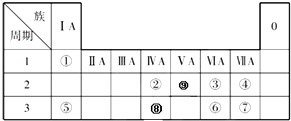
短周期元素W、X、Y和Z的原子序数依次增大.金属W是制备一种高效电池的重要材料,X原子的最外层电子数是内层电子数的2倍,元素Y的单质是常见的金属,可做海洋电池的负极材料.Z原子的质子数是同主族上一周期原子质子数的2倍.下列说法正确的是( )
| A、由金属W制备的高效电池可用NH4Cl溶液作电解质 |
| B、元素X与氢形成的化合物中不可能既有极性健又有非极性健 |
| C、元素Y、Z分别形成的简单离子,后者的离子半径较前者大 |
| D、元素Y、Z的最高价氧化物对应的水化物之间不能反应 |