题目内容
下列离子方程式书写正确的是( )
| A、偏铝酸钠中通足量的CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
| B、氯化铝溶液与足量氨水反应:Al3++4OH-═AlO2-+2H2O |
| C、氯化铝溶液与足量NaOH溶液反应:Al3++3OH-═Al(OH)3↓ |
| D、氧化铝和适量的烧碱溶液反应:Al2O3+2OH-═2AlO2-+H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.二氧化碳过量,反应生成的是碳酸氢根离子,不是碳酸根离子;
B.氨水碱性较弱,氯化铝和氨水反应生成氢氧化铝沉淀和氯化铵;
C.氢氧化钠足量,氢氧化铝沉淀溶解,反应生成偏铝酸钠和水;
D.氧化铝为两性氧化物,能够与强碱溶液反应生成偏铝酸钠和水.
B.氨水碱性较弱,氯化铝和氨水反应生成氢氧化铝沉淀和氯化铵;
C.氢氧化钠足量,氢氧化铝沉淀溶解,反应生成偏铝酸钠和水;
D.氧化铝为两性氧化物,能够与强碱溶液反应生成偏铝酸钠和水.
解答:
解:A.偏铝酸钠中通足量的CO2,反应生成氢氧化铝沉淀和碳酸氢根离子,正确的离子方程式为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,故A错误;
B.氨水不会溶解氢氧化铝,氯化铝和氨水反应生成氢氧化铝沉淀和氯化铵,正确的离子方程式为:Al3++3NH3?H2O=Al(OH)3↓+3NH4+,故B错误;
C.氯化铝溶液与足量NaOH溶液反应生成偏铝酸钠和水,正确的离子方程式为:Al3++4OH-═AlO2-+2H2O,故C错误;
D.氧化铝和适量的烧碱溶液反应生成偏铝酸钠和水,反应的离子方程式为:Al2O3+2OH-═2AlO2-+H2O,故D正确;
故选D.
B.氨水不会溶解氢氧化铝,氯化铝和氨水反应生成氢氧化铝沉淀和氯化铵,正确的离子方程式为:Al3++3NH3?H2O=Al(OH)3↓+3NH4+,故B错误;
C.氯化铝溶液与足量NaOH溶液反应生成偏铝酸钠和水,正确的离子方程式为:Al3++4OH-═AlO2-+2H2O,故C错误;
D.氧化铝和适量的烧碱溶液反应生成偏铝酸钠和水,反应的离子方程式为:Al2O3+2OH-═2AlO2-+H2O,故D正确;
故选D.
点评:本题考查了离子方程式的正误判断,为中等难度的试题,注意明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等;本题侧重铝及其化合物的性质考查,注意氢氧化铝、氧化钠能够溶液强碱溶液.

练习册系列答案
相关题目
乙醇分子内脱水的反应属于( )
| A、加聚反应 | B、取代反应 |
| C、加成反应 | D、消去反应 |
设NA为阿佛加德罗常数的数值,下列说法正确的是( )
| A、1L 1mol?L-1的Na2CO3 溶液中含有CO32-的数目为NA |
| B、25℃时pH=13的NaOH溶液中含有OH-的数目为0.1NA |
| C、一定条件下,2.3g的Na完全与O2反应生成3.6g产物时失去的电子数一定为0.1NA |
| D、1mol Fe与足量的稀HNO3反应,转移2NA个电子 |
下列金属的冶炼原理错误的是( )
A、MgCl2
| ||||
B、2Al2O3
| ||||
C、2Fe2O3
| ||||
D、2NaCl
|
把0.1mol铝投入100mL 3mol/L的NaOH溶液中充分反应,再滴入120mL 1mol/L的H2SO4溶液,其结果是
( )
( )
| A、溶液的pH>7 |
| B、得到澄清透明的溶液 |
| C、得到浑浊液体 |
| D、先有沉淀生成后逐渐溶解 |
强热绿矾晶体,除结晶水蒸发外,还发生如下化学反应:2FeSO4
Fe2O3+SO2↑+SO3↑.如果将生成的气体通入浓BaCl2溶液中,产生的现象是( )
| ||
| A、生成确BaSO4和BaSO3混合沉淀 |
| B、生成BaSO4沉淀,有SO2气体逸出 |
| C、生成BaSO4沉淀,有SO3气体逸出 |
| D、有SO2和SO3两种气体同时逸出 |
化学源于生活,同时又服务于生活,下列说法不合理的是( )
| A、田间焚烧秸秆污染环境,浪费资源 |
| B、泄露在海洋中的大量原油能被海洋生物迅速分解,不会导致生态灾难,不需要治理 |
| C、推广使用无磷洗涤剂,可有效减少水体的富营养化 |
| D、服用铬含量超标的药用胶囊会对从体健康造成危害 |
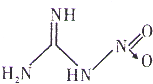 硝基胍是硝化纤维火药、硝化甘油火药的掺合剂、固体火箭推进剂的重要组分,其结构如图所示(“→”是一种特殊的共价单键).下列有关硝基胍的说法正确的是( )
硝基胍是硝化纤维火药、硝化甘油火药的掺合剂、固体火箭推进剂的重要组分,其结构如图所示(“→”是一种特殊的共价单键).下列有关硝基胍的说法正确的是( )| A、硝基胍分子中只含极性键,不含非极性键 |
| B、硝基胍中有C、H、O、N四种元素,属于氨基酸 |
| C、硝基胍分子中σ键与π键的个数比是5:1 |
| D、10.4 g该物质含有11×6.02×1023个原子 |