题目内容
短周期元素W、X、Y和Z的原子序数依次增大.金属W是制备一种高效电池的重要材料,X原子的最外层电子数是内层电子数的2倍,元素Y的单质是常见的金属,可做海洋电池的负极材料.Z原子的质子数是同主族上一周期原子质子数的2倍.下列说法正确的是( )
| A、由金属W制备的高效电池可用NH4Cl溶液作电解质 |
| B、元素X与氢形成的化合物中不可能既有极性健又有非极性健 |
| C、元素Y、Z分别形成的简单离子,后者的离子半径较前者大 |
| D、元素Y、Z的最高价氧化物对应的水化物之间不能反应 |
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:短周期元素W、X、Y和Z的原子序数依次增大,金属W是制备一种高效电池的重要材料,W为Li元素,X原子的最外层电子数是内层电子数的2倍,X有2个电子层,最外层电子数为4,故X为C元素,元素Y的单质是常见的金属,可做海洋电池的负极材料,Y为Al元素,Z原子的质子数是同主族上一周期原子质子数的2倍,故Z为S元素.
解答:
解:短周期元素W、X、Y和Z的原子序数依次增大,金属W是制备一种高效电池的重要材料,W为Li元素,X原子的最外层电子数是内层电子数的2倍,X有2个电子层,最外层电子数为4,故X为C元素,元素Y的单质是常见的金属,可做海洋电池的负极材料,Y为Al元素,Z原子的质子数是同主族上一周期原子质子数的2倍,故Z为S元素,
A.金属Li制备的高效电池用NH4Cl溶液作电解质,产生气体,容易发生极化现象,故A错误;
B.C元素与H元素形成的HC≡CH等既有极性健又有非极性健,故B错误;
C.元素Y、Z的简单离子分别为Al3+、S2-,S2-比Al3+多一个电子层,故S2-的离子半径较Al3+大,故C正确;
D.元素Y、Z的最高价氧化物对应的水化物分别为氢氧化铝、硫酸,二者反应生成硫酸铝与水,故D错误,
故选C.
A.金属Li制备的高效电池用NH4Cl溶液作电解质,产生气体,容易发生极化现象,故A错误;
B.C元素与H元素形成的HC≡CH等既有极性健又有非极性健,故B错误;
C.元素Y、Z的简单离子分别为Al3+、S2-,S2-比Al3+多一个电子层,故S2-的离子半径较Al3+大,故C正确;
D.元素Y、Z的最高价氧化物对应的水化物分别为氢氧化铝、硫酸,二者反应生成硫酸铝与水,故D错误,
故选C.
点评:本题考查元素推断、半径比较、原电池、物质性质与结构等,难度中等,注意C选项中半径比较.

练习册系列答案
相关题目
把0.1mol铝投入100mL 3mol/L的NaOH溶液中充分反应,再滴入120mL 1mol/L的H2SO4溶液,其结果是
( )
( )
| A、溶液的pH>7 |
| B、得到澄清透明的溶液 |
| C、得到浑浊液体 |
| D、先有沉淀生成后逐渐溶解 |
向澄清饱和石灰水中放入一小块钠,不可能出现的现象是( )
| A、钠熔化成光亮银白色的小球 |
| B、浮在液面快速游动 |
| C、液体底部出现银白色固体 |
| D、液面有水雾 |
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、1mol FeCl3完全水解转化为氢氧化铁胶体后能生成NA个胶粒 |
| B、标准状况下,2.24L NO2中含分子数有0.1NA个 |
| C、常温常压下,44g CO2中含有22NA个电子 |
| D、1mol?L-1 NaCl溶液含阴阳离子总数有2NA个 |
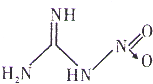 硝基胍是硝化纤维火药、硝化甘油火药的掺合剂、固体火箭推进剂的重要组分,其结构如图所示(“→”是一种特殊的共价单键).下列有关硝基胍的说法正确的是( )
硝基胍是硝化纤维火药、硝化甘油火药的掺合剂、固体火箭推进剂的重要组分,其结构如图所示(“→”是一种特殊的共价单键).下列有关硝基胍的说法正确的是( )| A、硝基胍分子中只含极性键,不含非极性键 |
| B、硝基胍中有C、H、O、N四种元素,属于氨基酸 |
| C、硝基胍分子中σ键与π键的个数比是5:1 |
| D、10.4 g该物质含有11×6.02×1023个原子 |
下列物质的水溶液中只存在一种分子的是( )
| A、Na2SO4 |
| B、NaHS |
| C、HNO3 |
| D、HClO |
下列离子方程式正确的是( )
| A、硫化亚铁溶于稀硝酸中:FeS+2H+═Fe2++H2S↑ |
| B、碘水中通入足量的SO2:I2+SO2+2H2O═2I-+SO42-+4H+ |
| C、NaHSO4溶液与Ba(OH)2溶液反应至中性:H++SO42-+Ba2++OH-═BaSO4↓+H2O |
| D、小苏打溶液中加足量Ba(OH)2溶液:2HCO3-+Ba2++2OH-═BaCO3↓+2H2O+CO32- |
对于苯乙烯(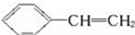 )的下列叙述:①使溴水反应褪色;②可发生加聚反应;③可溶于苯中;④可溶于水;⑤能发生取代反应;⑥所有的原子可能共平面.其中完全正确的是( )
)的下列叙述:①使溴水反应褪色;②可发生加聚反应;③可溶于苯中;④可溶于水;⑤能发生取代反应;⑥所有的原子可能共平面.其中完全正确的是( )
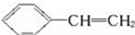 )的下列叙述:①使溴水反应褪色;②可发生加聚反应;③可溶于苯中;④可溶于水;⑤能发生取代反应;⑥所有的原子可能共平面.其中完全正确的是( )
)的下列叙述:①使溴水反应褪色;②可发生加聚反应;③可溶于苯中;④可溶于水;⑤能发生取代反应;⑥所有的原子可能共平面.其中完全正确的是( )| A、①②③⑤⑥ | B、①②⑤⑥ |
| C、①②④⑤ | D、①②③④⑤⑥ |
用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A、0.1mol Fe在0.1mol Cl2中充分燃烧,转移的电子数为0.3NA |
| B、标准状况下,11.2L CCl4所含分子数约为0.5NA |
| C、常温下,pH=13的NaOH溶液中,OH-的数目为0.1NA |
| D、常温、常压下,14g CO与N2的混合气含的原子数为NA |