题目内容
【题目】以水氯镁石(主要成分为MgCl26H2O)为原料生产碱式碳酸镁[Mgx(CO3)y(OH)zwH2O]的主要流程如图: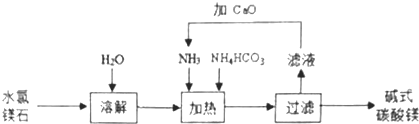
(1)上述流程中,滤液中溶质的主要成分(写化学式),向滤液中加入CaO的目的是 .
(2)上述流程中,检验“过滤”后碱式碳酸镁已洗涤干净的方法是 .
(3)已知高温煅烧碱式碳酸镁可得到MgO,取碱式碳酸镁4.66g,高温煅烧至恒重,得到固体2.00g和标准状况下CO20.896L.通过计算确定碱式碳酸镁的化学式(写出计算过程)。
【答案】
(1)NH4Cl;与滤液中NH4Cl反应产生NH3循环使用
(2)取最后一次洗涤液适量于试管中,滴加AgNO3溶液,若无白色浑浊出现,则证明已洗涤干净
(3)n(Mg2+)=n(MgO)= ![]() =0.05mol,n(CO32﹣)=n(CO2)=
=0.05mol,n(CO32﹣)=n(CO2)= ![]() =0.04mol,根据化合物中电荷守恒计算:n(OH﹣)=0.05mol×2﹣0.04mol×2=0.02mol, m(H2O)=4.66g﹣2.00g﹣0.04mol×44g/mol=0.9g, n(H2O)=
=0.04mol,根据化合物中电荷守恒计算:n(OH﹣)=0.05mol×2﹣0.04mol×2=0.02mol, m(H2O)=4.66g﹣2.00g﹣0.04mol×44g/mol=0.9g, n(H2O)= ![]() =0.05mol,结晶水的物质的量:n(H2O)═0.05mol﹣
=0.05mol,结晶水的物质的量:n(H2O)═0.05mol﹣ ![]() =0.04mol,
=0.04mol,
则得x:y:z:w=0.05:0.04:0.02:0.04=5:4:2:4碱式碳酸镁的化学式为:Mg5(CO3)4(OH)24H2O
【解析】解:以水氯镁石(主要成分为MgCl26H2O)为原料生产碱式碳酸镁[Mgx(CO3)y(OH)zwH2O],水溶解后得到氯化镁溶液,向氯化镁溶液中加入氨气、碳酸氢铵,加热,反应能生成碱式碳酸镁和氯化铵,过滤后滤液的主要溶质是氯化铵,铵根离子能和显碱性的物质反应生成氨气,氧化钙能和水反应生成显碱性的氢氧化钙溶液,可以用氧化钙和水反应生成的氢氧化钙,结合铵根离子生成氨气循环使用,(1)上述流程中,滤液中溶质的主要成分是NH4Cl,向滤液中加入CaO的目的是与滤液中NH4Cl 反应产生NH3循环使用,所以答案是:NH4Cl,与滤液中NH4Cl 反应产生NH3循环使用;(2)检验最后一次洗涤液中是否含有氯离子,可以加入硝酸银溶液观察是否生成白色沉淀,实验设计为:取最后一次洗涤液适量于试管中,滴加AgNO3溶液,若无白色浑浊出现,则证明已洗涤干净,所以答案是:取最后一次洗涤液适量于试管中,滴加AgNO3溶液,若无白色浑浊出现,则证明已洗涤干净;(3)n(Mg2+)=n(MgO)= ![]() =0.05 mol,n(CO32﹣)=n(CO2)=
=0.05 mol,n(CO32﹣)=n(CO2)= ![]() =0.04 mol,根据化合物中元素化合价代数和为零 n(OH﹣)=0.05 mol×2﹣0.04 mol×2=0.02mol, m (H2O)=4.66g﹣2.00g﹣0.04 mol×44 g/mol=0.9 g, n(H2O)=
=0.04 mol,根据化合物中元素化合价代数和为零 n(OH﹣)=0.05 mol×2﹣0.04 mol×2=0.02mol, m (H2O)=4.66g﹣2.00g﹣0.04 mol×44 g/mol=0.9 g, n(H2O)= ![]() =0.05 mol,结晶水的物质的量:n(H2O)═0.05 mol﹣
=0.05 mol,结晶水的物质的量:n(H2O)═0.05 mol﹣ ![]() =0.04 mol,则得x:y:z:w=0.05:0.04:0.02:0.04=5:4:2:4碱式碳酸镁的化学式为:Mg5(CO3)4(OH)24H2O,所以答案是:n(Mg2+)=n(MgO)=
=0.04 mol,则得x:y:z:w=0.05:0.04:0.02:0.04=5:4:2:4碱式碳酸镁的化学式为:Mg5(CO3)4(OH)24H2O,所以答案是:n(Mg2+)=n(MgO)= ![]() =0.05 mol,n(CO32﹣)=n(CO2)=
=0.05 mol,n(CO32﹣)=n(CO2)= ![]() =0.04 mol,根据化合物中元素化合价代数和为零 n(OH﹣)=0.05 mol×2﹣0.04 mol×2=0.02mol, m (H2O)=4.66g﹣2.00g﹣0.04 mol×44 g/mol=0.9 g, n(H2O)=
=0.04 mol,根据化合物中元素化合价代数和为零 n(OH﹣)=0.05 mol×2﹣0.04 mol×2=0.02mol, m (H2O)=4.66g﹣2.00g﹣0.04 mol×44 g/mol=0.9 g, n(H2O)= ![]() =0.05 mol,结晶水的物质的量:n(H2O)═0.05 mol﹣
=0.05 mol,结晶水的物质的量:n(H2O)═0.05 mol﹣ ![]() =0.04 mol,则得x:y:z:w=0.05:0.04:0.02:0.04=5:4:2:4碱式碳酸镁的化学式为:Mg5(CO3)4(OH)24H2O.
=0.04 mol,则得x:y:z:w=0.05:0.04:0.02:0.04=5:4:2:4碱式碳酸镁的化学式为:Mg5(CO3)4(OH)24H2O.