题目内容
【题目】下列关于碳酸钠和碳酸氢钠的比较中不正确的是( )
A.二者在水中的溶解度不同,碳酸氢钠的溶解度小于碳酸钠
B.二者热稳定性不同,碳酸钠的热稳定性大于碳酸氢钠
C.二者都能与盐酸反应放出二氧化碳气体,等质量时生成CO2量一样多
D.二者在一定条件下可以相互转化
【答案】C
【解析】
碳酸氢钠较不稳定,加热易分解;在相同温度下,在饱和碳酸钠溶液中通入二氧化碳气体,可观察到溶液变浑浊,生成碳酸氢钠,可说明碳酸钠溶解度大于碳酸氢钠,以此解答该题。
A.常温下相同的溶剂时,Na2CO3较NaHCO3易溶于水,因此二者的溶解度:碳酸钠>碳酸氢钠,A正确;
B.因2NaHCO3![]() Na2CO3+CO2↑+H2O,而碳酸钠加热不分解,碳酸钠稳定,B正确;
Na2CO3+CO2↑+H2O,而碳酸钠加热不分解,碳酸钠稳定,B正确;
C.Na2CO3相对分子质量是106,106g Na2CO3与足量盐酸反应产生1molCO2;NaHCO3的式量是84,84g NaHCO3与足量盐酸反应产生1molCO2;则106g NaHCO3与足量盐酸反应产生CO2的物质的量大于1mol;可见等质量的碳酸钠和碳酸氢钠,后者生成二氧化碳多,C错误;
D.加热条件下,碳酸氢钠固体能够转化成碳酸钠,反应的化学方程式为:2NaHCO3![]() Na2CO3+CO2↑+H2O;在溶液中,碳酸钠能够与二氧化碳反应生成碳酸氢钠,反应的化学方程式为:Na2CO3+CO2+H2O=2NaHCO3,碳酸钠和碳酸氢钠能够相互转化,D正确;
Na2CO3+CO2↑+H2O;在溶液中,碳酸钠能够与二氧化碳反应生成碳酸氢钠,反应的化学方程式为:Na2CO3+CO2+H2O=2NaHCO3,碳酸钠和碳酸氢钠能够相互转化,D正确;
故合理选项是C。

练习册系列答案
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案
相关题目
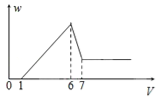
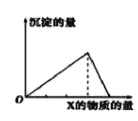
【题目】向物质Y中逐渐加入(或通入)X溶液,生成沉淀的量与加入X的物质的量关系如图所示,下表中符合图示情况的是
A | B | C | D | |
X | CO2 | HCl | NaOH | AlCl3 |
Y | Ca(OH)2 | NaAlO2 | AlCl3 | NaOH |
A.AB.BC.CD.D