题目内容
【题目】关于下图所示转化关系(X代表卤素),说法正确的是
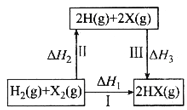
A.H2 (g)+X2(g)=2H(g)+2X(g) △H2<0
B.生成HX的反应热与途径有关,所以△H1≠△H2+△H3
C.若X分别表示Cl,Br,I,则过程Ⅱ吸收的热量依次增多
D.Cl2,Br2分别发生反应I,同一温度下的平衡常数分别为K1,K2,则K1 >K2
【答案】D
【解析】
试题A、断裂化学键是吸热过程,△H2>O,错误;B、反应焙变与起始物质和终态物质有关与变化途径无关,所以△H1=△H2+△H3,错误;C、氯、溴、碘单质中化学键的键能逐渐减小,所以过程Ⅱ吸收的热量依次减少,错误;D、因Cl2的氧化性大于Br2,所以Cl2与氢气化合的程度比Br2大,则C12 ,Br2分别发生反应I,同一温度下,氢气与Cl2反应的平衡常数大于氢气与Br2反应,故D正确。

练习册系列答案
相关题目
【题目】下表为元素周期表的一部分,用请化学用语回答有关问题:
IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
2 | E | F | ||||||
3 | A | C | D | G | R | |||
4 | B | H |
(1)C和H的元素符号是______和_______;
(2)表中A与F的氢化物反应的化学方程式___________,E的单质与其下一周期同族元素的最高价氧化物在高温下反应的化学方程式___________;最不活泼的元素________(填写元素符号)
(3)表中所列元素中最高价氧化物对应水化物碱性最强的是___________,酸性最强的是______ (填写化学式)
(4)表中能形成两性氢氧化物的元素是__________(填写元素符号),写出该元素的氢氧化物与A的最高价氧化物对应水化物反应的离子方程式__________________。