题目内容
【题目】某含C、H、O三种元素的有机物M的相对分子质量小于100,经燃烧分析实验测定该有机物中碳的质量分数为40%,氢的质量分数为6.7%。由此所得结论正确的是( )
A.M的分子式为CH2OB.M的实验式为CH3O
C.M不可能是2-羟基丙酸D.M可能是饱和一元羧酸
【答案】D
【解析】
由未知物中碳的质量分数、氢的质量分数可确定氧的质量分数,根据N=![]() 可计算出该物质中碳、氢、氧原子个数之比,以此解答该题。
可计算出该物质中碳、氢、氧原子个数之比,以此解答该题。
该有机物M中碳的质量分数为40%,氢的质量分数为6.7%,40%+6.7%<100%,说明该有机物中含有O元素,氧的质量分数为1-40%-6.7%=53.3%,则该有机物分子中碳、氢、氧三种元素的原子个数之比N(C):N(H):N(O)=![]() :
:![]() :
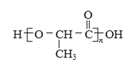
:![]() =1:2:1,物质M的实验式为CH2O,因M的相对分子质量小于100,则符合题意的M可能结构为HCHO、CH3COOH、CH3CH(OH)COOH等,分析选项物质,可知只有CH3COOH符合,乙酸是饱和一元羧酸,故正确选项为D。
=1:2:1,物质M的实验式为CH2O,因M的相对分子质量小于100,则符合题意的M可能结构为HCHO、CH3COOH、CH3CH(OH)COOH等,分析选项物质,可知只有CH3COOH符合,乙酸是饱和一元羧酸,故正确选项为D。

练习册系列答案
相关题目