题目内容
【题目】镍及其化合物用途广泛。某矿渣的主要成分是NiFe2O4(铁酸镍)、NiO、FeO、CaO、SiO2等,以下是从该矿渣中回收NiSO4的工艺路线:
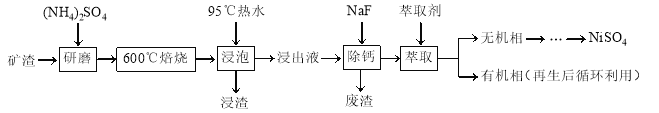
已知:(NH4)2SO4在350℃以上会分解生成NH3和H2SO4。NiFe2O4在焙烧过程中生成NiSO4、Fe2(SO4)3。锡(Sn)位于第五周期第ⅣA族。
(1)焙烧前将矿渣与(NH4)2SO4混合研磨,混合研磨的目的是______________。
(2)“浸泡”过程中Fe2(SO4)3生成FeO(OH)的离子方程式为______________,“浸渣”的成分除Fe2O3、FeO(OH)外还含有______________(填化学式)。
(3)为保证产品纯度,要检测“浸出液”的总铁量:取一定体积的浸出液,用盐酸酸化后,加入SnCl2将Fe3+还原为Fe2+,所需SnCl2的物质的量不少于Fe3+物质的量的________倍;除去过量的SnCl2后,再用酸性K2Cr2O7标准溶液滴定溶液中的Fe2+,还原产物为Cr3+,滴定时反应的离子方程式为______________。
(4)“浸出液”中c(Ca2+) = 1.0×10-3mol·L-1,当除钙率达到99%时,溶液中c(F-) = ________ mol·L-1。[已知Ksp (CaF2)=4.0×10-11]
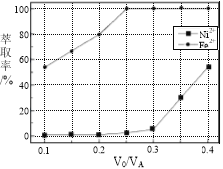
(5)本工艺中,萃取剂与溶液的体积比(V0/VA)对溶液中Ni2+、Fe2+的萃取率影响如图所示,V0/VA的最佳取值是________。
【答案】(1)增大接触面积,加快反应速率,使反应更充分;
(2)Fe3++2H2O![]() FeO(OH)↓+3H+,SiO2、CaSO4;
FeO(OH)↓+3H+,SiO2、CaSO4;
(3)0.5,Cr2O72-+6Fe2++14H+![]() 2Cr3++6Fe3++7H2O;(4)2.0×10-3;(5)0.25。
2Cr3++6Fe3++7H2O;(4)2.0×10-3;(5)0.25。
【解析】
试题分析:(1)混合研磨,增大接触面积,加快反应速率,使反应更充分;(2)放在95℃热水中浸泡,使Fe3+发生水解,即离子反应方程式为:Fe3++2H2O![]() FeO(OH)↓+3H+,SiO2不溶于水,Ca2+和SO42-生成微溶于水的CaSO4,因此浸渣中除Fe2O3、FeO(OH)外,还有SiO2和CaSO4;(3)根据得失电子数目守恒,n(Sn2+)×2=n(Fe3+)×1,解得n(Sn2+)/n(Fe3+)=0.5,K2Cr2O7→Cr3+,化合价降低3价,共降低6价,Fe2+→Fe3+,化合价升高1价,升高1价,最小公倍数为6,因此离子反应方程式为:Cr2O72-+6Fe2++14H+
FeO(OH)↓+3H+,SiO2不溶于水,Ca2+和SO42-生成微溶于水的CaSO4,因此浸渣中除Fe2O3、FeO(OH)外,还有SiO2和CaSO4;(3)根据得失电子数目守恒,n(Sn2+)×2=n(Fe3+)×1,解得n(Sn2+)/n(Fe3+)=0.5,K2Cr2O7→Cr3+,化合价降低3价,共降低6价,Fe2+→Fe3+,化合价升高1价,升高1价,最小公倍数为6,因此离子反应方程式为:Cr2O72-+6Fe2++14H+![]() 2Cr3++6Fe3++7H2O;(4)除钙后溶液中c(Ca2+)=1.0×10-3×1%mol·L-1=1.0×10-5mol·L-1,Ksp=c(Ca2+)×c2(F-),c(F-)=2.0×10-3mol·L-1;(5)要求Fe2+萃取率最低,Ni2+的萃取率最高,根据图像,最佳取值为0.25。
2Cr3++6Fe3++7H2O;(4)除钙后溶液中c(Ca2+)=1.0×10-3×1%mol·L-1=1.0×10-5mol·L-1,Ksp=c(Ca2+)×c2(F-),c(F-)=2.0×10-3mol·L-1;(5)要求Fe2+萃取率最低,Ni2+的萃取率最高,根据图像,最佳取值为0.25。

 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案