题目内容
15.下列说法正确的是( )| A. | 有一种第五形态的固体碳,这种新的碳结构称作“纳米泡沫”,它外形类似海绵,比重极小,并具有磁性.纳米泡沫碳与金刚石的转化是化学变化 | |
| B. | NO2能与水反应生成硝酸,所以NO2是酸性氧化物 | |
| C. | 铝粉和氧化镁粉末可以组成铝热剂发生铝热反应 | |
| D. | 某元素的气态氢化物能与其最高价氧化物对应的水化物发生化学反应,则该元素一定是N元素 |
分析 A.化学变化和物理变化的本质区别在于是否有新物质生成;
B.酸性氧化物是和碱反应生成盐和水的氧化物,反应为复分解反应;
C.镁比铝活泼;
D.最高价氧化物对应的水化物为HNO3,其氢化物为NH3,硝酸与氨气反应生成硝酸铵.
解答 解:A.纳米泡沫碳与金刚石的转化有新物质生成,是化学变化,故A正确;
B.NO2和水反应能生成硝酸和一氧化氮,发生的是氧化还原反应,与碱反应也是发生氧化还原反应,所以NO2不是酸性氧化物,故B错误;
C.镁的活泼性大于铝不能发生铝热反应,故C错误;
D.最高价氧化物对应的水化物为HNO3,其氢化物为NH3,硝酸与氨气反应生成硝酸铵,该元素一定是N元素,故D错误.
故选A.
点评 本题考查化学变化、元素的性质等,难度不大,试题侧重基础知识的考查,有利于培养学生灵活应用所学知识的能力.

练习册系列答案
相关题目
5.下列各组P、Q原子中,彼此的化学性质一定相似的是( )
| A. | P原子:1s2 Q原子:2s2 | |
| B. | P原子:M电子层上有2个电子 Q原子:N电子层上有2个电子 | |
| C. | P原子:2p能级上有1个未成对电子 Q原子:3p能级上有1个未成对电子 | |
| D. | P原子:最外电子层L层上只有一个空轨道 Q原子:3P能级上只有一个空轨道 |
6.化学为人类基本的生存需要、进而追求生活乃至生命质量的提升提供了重要的保障.但某些人的贪得无厌和对化学原理的滥用败坏了化学学科声誉,我们每个人都应该避免成为这样的人.下列科学史上的重要发现与发明,从原理上看与化学学科没有直接相关性的是( )
| A. | 1774年舍勒最早制得氯气,1820年前后漂白粉用于饮用水消毒 | |
| B. | 1869年门捷列夫发现元素周期律,使元素的性质更有规律可循 | |
| C. | 1902年哈伯开始对合成氨反应进行研究,工业化后提高了粮食产量 | |
| D. | 1942年费米进行了235U原子核裂变试验,从而开创原子能利用时代 |
3.下列实验现象预测正确的是( )
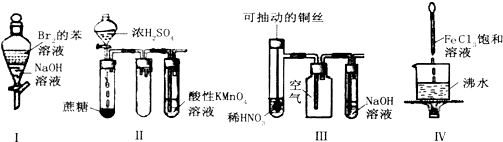

| A. | 实验Ⅰ:振荡后静置,上层溶液颜色保持不变 | |
| B. | 实验Ⅱ:酸性KMnO4溶液中无明显现象 | |
| C. | 实验Ⅲ:微热稀HNO3片刻,溶液中有气泡产生,广口瓶内始终保持无色 | |
| D. | 实验Ⅳ:继续煮沸溶液至红褐色,停止加热,当光束通过体系时可产生丁达尔效应 |
10.NA表示阿伏加德罗常数.下列说法中正确的是( )
| A. | 标准状况下,22.4LNO和11.2LO2混合后气体的分子总数为1.5NA | |
| B. | 6.2gNa2O和7.8gNa2O2混合物中所含有的阴离子数为0.3 NA | |
| C. | 14g乙烯和丙烯的混合物中,含有共用电子对数目为3×6.02×1023 | |
| D. | 18g D2O(重水)完全电解,转移6.02×1023个电子 |
20.LiFePO4新型锂离子动力电池以其独特的优势成为奥运会绿色能源的新宠.已知该电池放电时的电极反应式为:正极 FePO4+Li++e-═LiFePO4,负极 Li-e═Li+.下列说法中正确的是( )
| A. | 充电时电池反应为FePO4+Li=LiFePO4 | |
| B. | 充电时动力电池上标注“+”的电极应与外接电源的正极相连 | |
| C. | 放电时电池内部Li+向负极移动 | |
| D. | 所用的电解质(溶液)为水(溶液) |
7.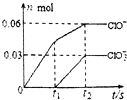 将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO${\;}_{3}^{-}$两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示.下列说法正确的是( )
将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO${\;}_{3}^{-}$两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示.下列说法正确的是( )
 将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO${\;}_{3}^{-}$两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示.下列说法正确的是( )
将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO${\;}_{3}^{-}$两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示.下列说法正确的是( )| A. | 苛性钾溶液中KOH的质量是4.94g | |
| B. | 反应中转移电子的物质的量是0.21mol | |
| C. | Cl-的物质的量为0.09mol | |
| D. | ClO${\;}_{3}^{-}$的生成是由于KOH过量引起的 |
4.下列离子方程式书写正确的是( )
| A. | 向NaHCO3溶液中加入足量的Ba(OH)2溶液:2HCO3-+Ba2++2OH-=BaCO3↓+2H2O+CO32- | |
| B. | 向亚硫酸钠溶液中滴入少量新制的氯水:3SO32-+Cl2+H2O=SO42-+2Cl-+2HSO3- | |
| C. | 电解KBr溶液时阴极的电极反应式为:K++e-=K | |
| D. | 将Fe2O3固体投入到少量HI溶液中:Fe2O3+6H++6I-=2Fe2++3I2+3H2O |
4.下列说法错误的是( )
| A. | 氧气和臭氧(O3)是氧元素的同素异形体 | |
| B. | 乙酸和甲酸甲酯是同分异构体 | |
| C. | 12C和13C互为同位素 | |
| D. | 软脂酸(C15H31COOH)和油酸(C17H33COOH)是同系物 |