题目内容
【题目】请阅读下列材料,完成下面小题。
联合国将2019年定为“国际化学元素周期表年”以纪念门捷列夫发现元素周期律150周年。元素周期律把元素及其化合物纳入一个统一的理论体系,为系统研究元素及其化合物提供了科学方法,为发现和探索新元素、新物质提供了有效思路。
1. 为纪念门捷列夫,科学家将1955年人工合成的一种新元素用符号“Md”表示,中文命名为“钔”。核素![]() Md的中子数为(______)
Md的中子数为(______)
A. 101 B. 359 C. 258 D. 157
2. O和S都属于元素周期表ⅥA元素,它们原子结构中相同的是(______)
A. 质子数 B. 电子层数 C. 电子数 D. 最外层电子数
3. 锂是第2周期ⅠA族元素,下列有关锂元素性质推测正确的是(______)
A. 金属性比钠弱
B. 最高化合价为+2
C. 单质与水的反应比钠更剧烈
D. 原子半径比钠的大
【答案】D D A
【解析】
【1】
核素![]() Md的左下角数字101表示质子数,左上角数字258表示质量数,对于一个核素来说,质量数=质子数+中子数,所以中子数=质量数-质子数=258-101=157,故选D。
Md的左下角数字101表示质子数,左上角数字258表示质量数,对于一个核素来说,质量数=质子数+中子数,所以中子数=质量数-质子数=258-101=157,故选D。
【2】
A.O和S的质子数分别为8和16,二者的质子数不相等,A不合题意;
B.O和S的电子层数分别为2和3,二者的电子层数不相等,B不合题意;
C.O和S的电子数分别为8和16,二者的电子数不相等,C不合题意;
D.O和S的最外层电子数都为6,二者的最外层电子数相等,D符合题意;
故选D。
【3】
A.锂与钠是同主族元素,锂在钠的上方,金属性比钠弱,A正确;
B.锂是第二周期ⅠA族元素,最外层只有1个电子,最高化合价为+1价,B不正确;
C.锂的金属性比钠弱,所以单质与水的反应比钠慢,C不正确;
D.锂与钠同主族,且比钠少1个电子层,所以原子半径比钠小,D不正确;
故选A。

 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案【题目】下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
族 周期 | IA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(1)⑧的原子结构示意图为_________;
(2)②的气态氢化物分子的结构式为___________,②和⑦的气态氢化物的稳定性相比,其中较弱的是____ (用该氢化物的化学式表示);
(3)②、③的最高价含氧酸的酸性由强到弱的顺序是____(填化学式);
(4)⑤、⑥元素的金属性强弱依次为___________(填“增大”、“减小”或“不变”);
(5)④、⑤、⑥的形成的简单离子半径依次_________(填“增大”、“减小”或“不变”);
(6)①、④、⑤元素可形成既含离子键又含共价键的化合物,写出它的电子式:_____。
【题目】某研究性学习小组利用H2C2O4溶液和酸性KMnO4溶液之间的反应来探究“外界条件改变对化学反应速率的影响”,实验如下,下列说法错误的是( )
实验 序号 | 实验温度T/K | 参加反应的物质 | 溶液颜色褪至无色时所需时间t/s | ||||
KMnO4溶液(含硫酸) | H2C2O4溶液 | H2O | |||||
V/mL | c/mol·L-1 | V/mL | c/mol·L-1 | V/mL | |||
A | 293 | 4 | 0.02 | 6 | 0.1 | 0 | 6 |
B | 293 | 4 | 0.02 | 4 | 0.1 | V1 | 8 |
C | T1 | 4 | 0.02 | 6 | 0.1 | 0 | 5 |
A.时间t的意义是,从溶液混合到KMnO4颜色褪去的时间
B.实验C中5s内平均反应速率v(KMnO4)=1.6×10-3molL-1s-1
C.实验A和B是探究
D.实验A和C是探究温度对反应速率的影响,则T1>293
【题目】钠、铝是两种重要的金属,其单质及化合物在人们的日常生活、生产及科学研究中具有广泛的用途。回答下列问题:
(1)基态铝原子的电子排布图是____________________。
(2)与Al3+具有相同的电子层结构的简单阴离子有__________(填离子符号),其中形成这些阴离子的元素中,电负性最强的是__________(填元素符号,下同),第一电离能最小的是__________。
(3)Al、Cl的电负性如下表:
元素 | Al | Cl |
电负性 | 1.5 | 3.0 |
则AlCl3为________晶体(填晶体类型);AlCl3升华后蒸气的相对分子质量约为267,则该蒸气分子的结构式是____________(标明配位键)。
(4)氢化铝钠(NaAlH4)是重要的有机合成中还原剂。
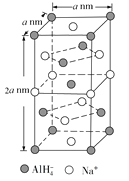
①![]() 的空间构型为____________。
的空间构型为____________。
②NaAlH4的晶胞如下图所示,与Na+紧邻且等距的![]() 有________个;NaAlH4晶体的密度为________g/cm3(用含a 的代数式表示,NA代表阿伏加德罗常数)。
有________个;NaAlH4晶体的密度为________g/cm3(用含a 的代数式表示,NA代表阿伏加德罗常数)。