题目内容
1.下列物质不属于分散系的是( )| A. | 冰水混合物 | B. | 氯化钠溶液 | C. | 泥浆 | D. | 淀粉溶液 |
分析 一种(或多种)物质分散在另一种(或多种)物质中所形成的体系称为分散体系,属于混合物.被分散的物质为分散质,起容纳分散质作用的为分散剂.
解答 解:A.冰水混合物的成分是水,是纯净物,不属于分散系,故A正确;
B.氯化钠溶液属于分散系,故B错误;
C.泥浆是浊液,属于分散系,故C错误;
D.淀粉溶液是胶体,属于分散系,故D错误.
故选A.
点评 本题考查分散系概念,难度较小,注意把握分散系概念,分散质分散于分散剂中,属于混合物,但混合物不一定是分散系.

练习册系列答案
相关题目
11.不能用影响化学速率的条件(浓度、压强、温度、催化剂)来解释的是( )
| A. | 锌分别与相同浓度的盐酸和醋酸作用产生H2的速率盐酸快 | |
| B. | H2S在空气中燃烧是淡蓝色火焰,在纯氧中燃烧呈蓝紫色火焰 | |
| C. | 用加热的方法将水中的氮气、氧气逐出 | |
| D. | 面粉加工厂内充满粉尘,遇火焰发生爆炸 |
12.某硫酸溶液的密度为1.48g/cm3,溶质质量分数为49%.该溶液的溶质的物质的量浓度是( )
| A. | 0.0074mol/L | B. | 0.74mol/L | C. | 7.4mol/L | D. | 4.9mol/L |
9.某稀溶液仅含Fe2+、Na+、Al3+、Ba2+、SO42-、NO3-、Cl-中的4种离子,所含离子的物质的量均为1mol.若向该溶液中加入适量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解).下列说法正确的是( )
| A. | 若向该溶液中加入足量的NaOH溶液,充分反应后,过滤、洗涤、灼烧,最终所得固体的质量为72g | |
| B. | 若向该溶液中加入过量的稀硫酸,溶液颜色会变成浅绿色 | |
| C. | 若向该溶液中加入过量的稀硫酸和KSCN溶液,溶液不显血红色 | |
| D. | 若向该溶液中加入过量的稀硫酸,产生的气体在标况下的体积约为7.467 L |
16. 学习小组设计了如图实验(部分装置),将氯气依次通过下列装置以验证氯气的性质:
学习小组设计了如图实验(部分装置),将氯气依次通过下列装置以验证氯气的性质:
(1)通入氯气后,A中的现象是溶液变蓝色.C装置中发生反应的离子方程式为:2Fe2++Cl2═2Fe3++2Cl-.
(2)通入氯气一段时间后,洗气瓶B溶液中有一部分SO32-氧化成SO42-.设计试验方案,检验洗气瓶B溶液中Cl-和SO42-的存在.在答题卡上补充填写出实验步骤、预期现象和结论.
限选试剂及仪器:2mol/LHCl、2mol/LHNO3、1mol/LBaCl2溶液、lmol/LBa(NO3)2溶液、0.1mol/LAgNO3溶液、澄清石灰水、试管、胶头滴管.
(3)为准确测定通入氯气一段时间后剩余FeCl2的物质的量.实验如下:
①配制250mL 溶液:取洗气瓶C中全部溶液准确配制250mL溶液.
②滴定:准确量取25.00ml所配溶液于锥形瓶中,将0.1980mol/LKMnO4溶液装入酸式滴定管,滴定至终点,记录数据.重复滴定2次.平均消耗KMnO4溶液V mL.(反应式:Fe2++MnO4-+H+-Fe3++Mn2++H2O,未配平)
③计算250mL溶液中FeCl2的物质的量=$\frac{250}{25.00}$×0.1980×V×10-3×5或10×0.1980×V×10-3×5mol(只列出算式,不做运算).
 学习小组设计了如图实验(部分装置),将氯气依次通过下列装置以验证氯气的性质:
学习小组设计了如图实验(部分装置),将氯气依次通过下列装置以验证氯气的性质:(1)通入氯气后,A中的现象是溶液变蓝色.C装置中发生反应的离子方程式为:2Fe2++Cl2═2Fe3++2Cl-.
(2)通入氯气一段时间后,洗气瓶B溶液中有一部分SO32-氧化成SO42-.设计试验方案,检验洗气瓶B溶液中Cl-和SO42-的存在.在答题卡上补充填写出实验步骤、预期现象和结论.
限选试剂及仪器:2mol/LHCl、2mol/LHNO3、1mol/LBaCl2溶液、lmol/LBa(NO3)2溶液、0.1mol/LAgNO3溶液、澄清石灰水、试管、胶头滴管.
| 实验步骤 | 预期现象和结论 |
步骤1:取适量洗气瓶B中溶液于试管A中,滴加滴加过量2mol/LHCl(1分)和1mol/LBaCl2溶液,振荡. | 若产生的白色沉淀,则洗气瓶B溶液中存在SO42-. |
步骤2:另取适量洗气瓶B中溶液于试管B中,滴加滴加入过量lmol/LBa(NO3)2溶液,振荡,静置. | 产生白色沉淀. |
步骤3:取步骤2后试管B中的上层清液于试管C中, 滴加0.1mol/LAgNO3溶液和过量的2mol/LHNO3,振荡. | 若产生白色沉淀,则洗气瓶B溶液中存在氯离子. |
①配制250mL 溶液:取洗气瓶C中全部溶液准确配制250mL溶液.
②滴定:准确量取25.00ml所配溶液于锥形瓶中,将0.1980mol/LKMnO4溶液装入酸式滴定管,滴定至终点,记录数据.重复滴定2次.平均消耗KMnO4溶液V mL.(反应式:Fe2++MnO4-+H+-Fe3++Mn2++H2O,未配平)
③计算250mL溶液中FeCl2的物质的量=$\frac{250}{25.00}$×0.1980×V×10-3×5或10×0.1980×V×10-3×5mol(只列出算式,不做运算).
6.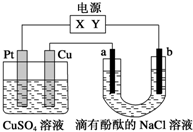 如图,a、b是石墨电极,通电一段时间后,b极附近溶液显红色.下列说法正确的是( )
如图,a、b是石墨电极,通电一段时间后,b极附近溶液显红色.下列说法正确的是( )
 如图,a、b是石墨电极,通电一段时间后,b极附近溶液显红色.下列说法正确的是( )
如图,a、b是石墨电极,通电一段时间后,b极附近溶液显红色.下列说法正确的是( )| A. | Pt为阴极,Cu为阳极 | |
| B. | b极的电极反应式是2H++2e-═H2↑ | |
| C. | 电解过程中CuSO4溶液的pH逐渐增大 | |
| D. | Pt极上有6.4 g Cu析出时,b极产生2.24 L(标准状况)气体 |
13.在实验室可利用浓盐酸与二氧化锰共热制氯气,制备装置中须安装分液漏斗而不能使用长颈漏斗,有关原因叙述错误的是( )
| A. | 防止氯气通过漏斗扩散到空气中造成污染 | |
| B. | 便于控制加入浓盐酸的量 | |
| C. | 因长颈漏斗加热时容易破裂 | |
| D. | 尽量避免HC1挥发到空气中 |
10.某温度下,某溶液中c(H+)=10-6 mol/L.则该溶液显( )
| A. | 酸性 | B. | 酸性或中性 | C. | 碱性 | D. | 无法判断 |
11.一定质量的某种有机物和足量金属钠反应,得到VA L气体,相同质量的该有机物与足量Na2CO3溶液反应,可得VB L气体,已知同温同压下VA≠VB.则该有机物可能是( )
| A. | CH3CH(OH)COOH | B. |  | ||
| C. | CH3CH2COOH | D. | HOOC-COOH |