题目内容
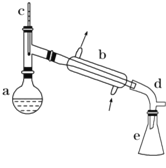
【题目】醇脱水是制取烯烃的常用方法,实验室以环己醇为原料制取环己烯的实验装置如图所示。
反应的化学方程式:
合成反应:
在a中加入40g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1mL浓硫酸,b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90℃。
分离提纯:
反应粗产物倒入分液漏斗中,分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙,最终通过蒸馏得到纯净环己烯20g。
可能用到的有关数据如下:
相对分子质量 | 密度/(g·cm-3) | 沸点/℃ | 溶解性 | |
环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
回答下列问题:
(1)装置b的名称是___________
(2)加入碎瓷片的作用是_________
(3)本实验中最容易产生的副反应的化学方程式为______________
(4)分离提纯过程中加入无水氯化钙的目的是________________
(5)本实验所得到的环己烯产率是____(填正确答案标号)
A.41% B.50% C.61% D.70%
【答案】(直型)冷凝管 防止液体暴沸 ![]() 除水(除醇)或干燥环己烯 C
除水(除醇)或干燥环己烯 C
【解析】
(1)根据装置图回答仪器名称;
(2)碎瓷片可以防止在加热过程中产生暴沸现象;
(3)加热过程中,环己醇除可发生消去反应生成环己烯外,还可以发生取代反应生成二环己醚;
(4)氯化钙可以作干燥剂;
(5)产率=![]()
(1)根据装置图,b的名称是(直型)冷凝管;
(2)碎瓷片的存在可以防止在加热过程中产生暴沸现象;
(3)加热过程中,环己醇除可发生消去反应生成环己烯外,还可以发生取代反应生成二环己醚,反应方程式是![]() ;
;
(4)氯化钙可以作干燥剂,分离提纯过程中加入无水氯化钙的目的是干燥环己烯;
(5)设环己烯的理论产量是xg
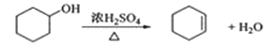
100g 82g
40g xg
![]()
X=32.8g
产率=![]() =
=![]() 61%,故选C。
61%,故选C。

 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案