题目内容
16.按要求写出离子方程式.(1)用氢氧化钠溶液吸收有毒的氯气Cl2+2OH-=Cl-+ClO-+H2O.
(2)红热的碳单质放入浓硝酸中产生大量的红棕色气体4H++4NO3-+C$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O.
(3)NaOH溶液和少量Ca(HCO3)2反应Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32-.
(4)过量的铁与稀硝酸的反应3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O.
分析 (1)氢氧化钠与氯气反应生成氯化钠、次氯酸钠和水;
(2)二者反应生成二氧化碳、二氧化氮和水;
(3)NaOH溶液和少量Ca(HCO3)2反应生成碳酸钙、碳酸钠和水;
(4)反应生成硝酸亚铁、一氧化氮和水;
解答 解:(1)氢氧化钠与氯气反应生成氯化钠、次氯酸钠和水,离子方程式:Cl2+2OH-=Cl-+ClO-+H2O;
故答案为:Cl2+2OH-=Cl-+ClO-+H2O;
(2)红热的碳单质放入浓硝酸中产生大量的红棕色气体,离子方程式:4H++4NO3-+C$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O;
故答案为:4H++4NO3-+C$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O;
(3)NaOH溶液和少量Ca(HCO3)2反应生成碳酸钙、碳酸钠和水,离子方程式:Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32-;
故答案为:Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32-;
(4)过量的铁与稀硝酸的反应生成硝酸亚铁、一氧化氮和水,离子方程式:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O;
故答案为:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O;
点评 本题考查离子方程式的书写,为高考高频考点,注意把握物质的性质以及离子方程式的书写方法,难度不大.

练习册系列答案
相关题目
6.已知下述三个实验均能发生化学反应.①将铁钉放入硫酸铜溶液中;②向硫酸亚铁溶液中滴入几滴浓硝酸;③将铁钉放入氯化铁溶液中.下列判断正确的是( )
| A. | 实验①和③中的铁钉只作还原剂 | |
| B. | 上述实验证明氧化性:Fe3+>Fe2+>Cu2+ | |
| C. | 实验②中Fe2+既显氧化性又显还原性 | |
| D. | 实验③中反应的离子方程式为2Fe+Fe3+═3Fe2+ |
7.如图是某化学反应的示意图(“○”与“o”分别代表不同元素原子),该反应可能为( )


| A. | 氢气的燃烧 | B. | 水的电解 | C. | 甲烷的燃烧 | D. | 一氧化碳的燃烧 |
4.1mol/L H2SO4的含义是( )
| A. | 1L水中含有1molH2SO4 | B. | 1L溶液中含有1molH+ | ||
| C. | 1LH2SO4溶液中含98g H2SO4 | D. | 将98g H2SO4溶于1L水配成溶液 |
1.某固体混合物可能由Al、(NH4)2SO4、MgCl2、FeCl2、AlCl3中的两种或多种组成,现对该混合物做如下实验,所得现象和有关数据如图所示(气体体积数据已换算成标准状况下的体积):

关于该固体混合物,下列说法正确的是( )

关于该固体混合物,下列说法正确的是( )
| A. | 一定含有Al,其质量为4.5g | |
| B. | 一定含有(NH4)2SO4和MgCl2,且物质的量相等 | |
| C. | 一定含有MgCl2和FeCl2 | |
| D. | 一定不含FeCl2,可能含有MgCl2和AlCl3 |
7.阿司匹林是一种历史悠久的解热镇痛药,学名为乙酰水杨酸,结构简式为 .某探究小组在实验室探究阿司匹林的合成,主要原料是水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O],制备基本实验流程如下:
.某探究小组在实验室探究阿司匹林的合成,主要原料是水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O],制备基本实验流程如下:

已知:①乙酰水杨酸是白色晶体,易溶于乙醇、乙醚,在128~135℃易分解.
②主要试剂和产品的其它物理常数
请根据以上信息回答下列问题:
(1)写出水杨酸与醋酸酐制备阿司匹林的化学方程式 .
.
(2)制备阿司匹林主反应时,仪器必须干燥的原因是防止醋酸酐与水反应.
(3)合成阿司匹林主反应时,最合适的加热方法是水浴加热,除酒精灯外,该加热装置还需要的玻璃仪器有烧杯(或水浴锅)、温度计.
(4)提纯粗产品时加入饱和NaHCO3溶液至没有CO2产生为止,再抽滤(即减压过滤),结合提纯流程回答加饱和NaHCO3溶液的目的是使乙酰水杨酸与NaHCO3溶液反应,转化为易溶于水的乙酰水杨酸钠,便于分离.
(5)最终所得产品可能仍含有少量水杨酸,检验含有水杨酸的操作和现象是取少量粗产品于试管中,加适量乙醇(或蒸馏水)溶解,滴加几滴FeCl3溶液,若呈紫色则含水杨酸,若无紫色出现,说明产品中不含水杨酸..
 .某探究小组在实验室探究阿司匹林的合成,主要原料是水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O],制备基本实验流程如下:
.某探究小组在实验室探究阿司匹林的合成,主要原料是水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O],制备基本实验流程如下:
已知:①乙酰水杨酸是白色晶体,易溶于乙醇、乙醚,在128~135℃易分解.
②主要试剂和产品的其它物理常数
| 名称 | 相对分子质量 | 熔点或沸点(℃) | 水溶性 |
| 水杨酸 | 132 | 158(熔点) | 微溶 |
| 醋酸酐 | 102 | 139.4(沸点) | 与水反应 |
| 乙酰水杨酸 | 180 | 135(熔点) | 微溶 |
(1)写出水杨酸与醋酸酐制备阿司匹林的化学方程式
 .
.(2)制备阿司匹林主反应时,仪器必须干燥的原因是防止醋酸酐与水反应.
(3)合成阿司匹林主反应时,最合适的加热方法是水浴加热,除酒精灯外,该加热装置还需要的玻璃仪器有烧杯(或水浴锅)、温度计.
(4)提纯粗产品时加入饱和NaHCO3溶液至没有CO2产生为止,再抽滤(即减压过滤),结合提纯流程回答加饱和NaHCO3溶液的目的是使乙酰水杨酸与NaHCO3溶液反应,转化为易溶于水的乙酰水杨酸钠,便于分离.
(5)最终所得产品可能仍含有少量水杨酸,检验含有水杨酸的操作和现象是取少量粗产品于试管中,加适量乙醇(或蒸馏水)溶解,滴加几滴FeCl3溶液,若呈紫色则含水杨酸,若无紫色出现,说明产品中不含水杨酸..
4.CoCl2•6H2O是一种饲料营养强化剂,一种利用水钴矿[主要成分为Co2O3、Co(OH)3,还含少量Fe2O3、•Al2O3、MnO等]制取CoCl2•6H2O的工艺流程如下:
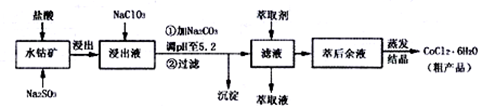
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见表.
(1)盐酸的作用是溶解矿石,提供酸性环境,Na2SO3的作用是(文字描述)将Fe3+、Co3+还原.
(2)NaClO3加入浸出液后生成NaCl,写出反应的离子方程式ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O.
(3)加Na2CO3调pH至5.2的目的是为完全沉淀Fe3+、Al3+.
(4)萃取剂对金属离子的萃取率与pH的关系如图1,萃取剂的作用是除去溶液中的Mn2+,其使用的适宜pH范围是C.A.1.0~2.0 B.2.0~2.5 C.3.0~3.5 D 4.0~4.5
(5)取部分加入萃取剂后的混合液,在实验室按流程图获得粗产品.
①使用分液漏斗前要检漏,是检查玻璃塞、旋塞芯是否漏水,若发现其中一处漏水,必要的操作或做法是若发现玻璃塞处漏水,更换分液漏斗,若发现旋塞芯处漏水,则用纸或干布擦净旋塞或旋塞孔,在旋塞芯上涂一层薄薄的润滑脂,将旋塞芯塞进旋塞内,旋转数圈,使润滑脂均匀分布后将旋塞关闭好.(只写出其中一种漏水对应的操作或做法)
②在蒸发过程中为防止产生杂质或脱水,当较多晶体析出时,改为抽滤得到晶体.
写出抽滤装置(如图2)中指定仪器的名称:A安全瓶,B抽气泵.
下列抽滤操作或说法正确的是ABE
A.用蒸馏水润湿滤纸,微开水龙头,抽气使滤纸紧贴在漏斗瓷板上
B.用倾析法转移溶液,开大水龙头,待溶液快流尽时再转移沉淀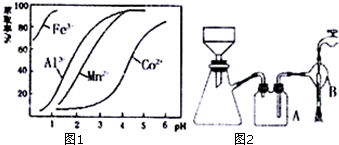
C.注意吸滤瓶内液面高度,当接近支管口位置时,拨掉橡皮管,滤液从支管口倒出
D.用抽滤洗涤沉淀时,应开大水龙头,使洗涤剂快速通过沉淀物,以减少沉淀物损失
E.抽滤不宜用于过滤胶状或颗粒太小的沉淀
用少量蒸馏水洗涤晶体,判断晶体是否洗净的具体操作是用洁净的铂丝蘸取最后一次洗涤液在酒精灯火焰上灼烧,如果看到黄色火焰,说明没有洗净,否则已洗净.

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见表.
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)2 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(2)NaClO3加入浸出液后生成NaCl,写出反应的离子方程式ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O.
(3)加Na2CO3调pH至5.2的目的是为完全沉淀Fe3+、Al3+.
(4)萃取剂对金属离子的萃取率与pH的关系如图1,萃取剂的作用是除去溶液中的Mn2+,其使用的适宜pH范围是C.A.1.0~2.0 B.2.0~2.5 C.3.0~3.5 D 4.0~4.5
(5)取部分加入萃取剂后的混合液,在实验室按流程图获得粗产品.
①使用分液漏斗前要检漏,是检查玻璃塞、旋塞芯是否漏水,若发现其中一处漏水,必要的操作或做法是若发现玻璃塞处漏水,更换分液漏斗,若发现旋塞芯处漏水,则用纸或干布擦净旋塞或旋塞孔,在旋塞芯上涂一层薄薄的润滑脂,将旋塞芯塞进旋塞内,旋转数圈,使润滑脂均匀分布后将旋塞关闭好.(只写出其中一种漏水对应的操作或做法)
②在蒸发过程中为防止产生杂质或脱水,当较多晶体析出时,改为抽滤得到晶体.
写出抽滤装置(如图2)中指定仪器的名称:A安全瓶,B抽气泵.
下列抽滤操作或说法正确的是ABE
A.用蒸馏水润湿滤纸,微开水龙头,抽气使滤纸紧贴在漏斗瓷板上
B.用倾析法转移溶液,开大水龙头,待溶液快流尽时再转移沉淀

C.注意吸滤瓶内液面高度,当接近支管口位置时,拨掉橡皮管,滤液从支管口倒出
D.用抽滤洗涤沉淀时,应开大水龙头,使洗涤剂快速通过沉淀物,以减少沉淀物损失
E.抽滤不宜用于过滤胶状或颗粒太小的沉淀
用少量蒸馏水洗涤晶体,判断晶体是否洗净的具体操作是用洁净的铂丝蘸取最后一次洗涤液在酒精灯火焰上灼烧,如果看到黄色火焰,说明没有洗净,否则已洗净.
5.在一密闭容器中加入A和B,各物质的物质的量浓度随着反应的进行,如图所示.下列说法不正确的是( )

| A. | 该反应的化学方程式为5A+4B?4C | |
| B. | 2min时,该反应达到平衡,此时A、B、C的浓度比为5:4:4 | |
| C. | 用B的浓度变化表示0-2min时间内的速率为2mol/(L•min) | |
| D. | 2min前,正反应速率逐渐减小,逆反应速率逐渐增大,但是正反应速率大于逆反应速率 |