题目内容
【题目】按要求回答下列问题:
(1)将28.5 g氯化镁溶于水配成的500 mL溶液中Cl浓度是 ,写出氯化镁的电离方程式 。
(2)已知m mol某气体的质量为a g,则b g该气体在标准状况下的体积为 L。
(3)某Al2(SO4)3溶液V mL中含有Al3+a g,取出![]() mL溶液稀释成V mL后,
mL溶液稀释成V mL后,![]() 的物质的量浓度为 (用含a、V的代数式表示,化简到最简整数比)。
的物质的量浓度为 (用含a、V的代数式表示,化简到最简整数比)。
(4)以下物质:①NaCl晶体 ②液态SO3 ③液态的醋酸 ④铝 ⑤BaSO4固体 ⑥蔗糖(C12H22O11) ⑦酒精(C2H5OH) ⑧熔融KNO3,其中属于电解质的是 (填编号,下同),能导电的是 。
【答案】(7分)(1)1.2 mol/L(1分) MgCl2![]() Mg2++2Cl(1分)
Mg2++2Cl(1分)
(2)22.4mb/a(1分)
(3)![]() mol/L(2分)
mol/L(2分)
(4)①③⑤⑧(1分) ④⑧(1分)
【解析】(1)28.5 g氯化镁的物质的量为![]() =0.3 mol,其中Cl的物质的量为0.3 mol×2 =0.6 mol,将该氯化镁溶于水配成的500 mL溶液中Cl浓度为
=0.3 mol,其中Cl的物质的量为0.3 mol×2 =0.6 mol,将该氯化镁溶于水配成的500 mL溶液中Cl浓度为![]() =1.2 mol/L;氯化镁的电离方程式为MgCl2
=1.2 mol/L;氯化镁的电离方程式为MgCl2![]() Mg2++2Cl。
Mg2++2Cl。
(2)m mol某气体的质量为a g,则该气体摩尔质量为![]() =
=![]() g/mol,b g该气体的物质的量为
g/mol,b g该气体的物质的量为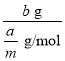 =
=![]() mol。在标准状况下,该气体的体积为
mol。在标准状况下,该气体的体积为![]() mol×22.4 L/mol=
mol×22.4 L/mol=![]() L。
L。
(3)a g Al3+的物质的量为![]() =
=![]() mol,溶液中n(Al3+)∶n(
mol,溶液中n(Al3+)∶n(![]() )=2∶3,V L溶液中n(
)=2∶3,V L溶液中n(![]() )=
)=![]() mol×
mol×![]() =
=![]() mol,故
mol,故![]() mL溶液中n(
mL溶液中n(![]() )=
)=![]() mol×
mol×![]() =
=![]() mol,故稀释后溶液中
mol,故稀释后溶液中![]() 物质的量浓度为
物质的量浓度为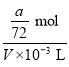 =
=![]() mol/L=
mol/L=![]() mol/L。
mol/L。
(4)所给物质中,属于电解质的有①③⑤⑧,能导电的有④⑧。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目