题目内容
T℃时,某一气态平衡体系中含有X(g)、Y(g)、Z(g)、W(g)四种物质,此温度下发生反应的平衡常数表达式为: ,有关该平衡体系的说法正确的是
,有关该平衡体系的说法正确的是
A.该反应可表示为X(g) + 2Y(g) 2Z(g) + 2W(g) 2Z(g) + 2W(g) |
| B.减小X浓度,平衡向逆反应方向移动,平衡常数K减小 |
| C.增大反应容器的压强,该反应速率一定增大 |
| D.升高温度,W(g)体积分数增加,则正反应是放热反应 |
D
解析试题分析:A.由于化学平衡常数是可逆反应达到平衡状态时各生成物浓度幂指数的乘积与各反应物浓度幂指数乘积的比。所以该反应可表示为2Z(g) + 2W(g)  X(g) + 2Y(g)。错误。B. 减小X浓度,平衡向正反应方向移动,但是由于反应的温度不变,所以化学平衡常数K不变。错误。C.若容器的容积不变,向容器内冲入与体系无关的气体而增大反应容器的压强,由于各物质的浓度没变,所以该反应速率不变;若缩小容器的容积,使物质的浓度增大,则化学反应速率加快。错误。D.根据平衡移动原理:升高温度,化学平衡向吸热反应方向移动。由于W(g)体积分数增加,则升高温度平衡逆向移动逆反应为吸热反应。则正反应是放热反应。正确。
X(g) + 2Y(g)。错误。B. 减小X浓度,平衡向正反应方向移动,但是由于反应的温度不变,所以化学平衡常数K不变。错误。C.若容器的容积不变,向容器内冲入与体系无关的气体而增大反应容器的压强,由于各物质的浓度没变,所以该反应速率不变;若缩小容器的容积,使物质的浓度增大,则化学反应速率加快。错误。D.根据平衡移动原理:升高温度,化学平衡向吸热反应方向移动。由于W(g)体积分数增加,则升高温度平衡逆向移动逆反应为吸热反应。则正反应是放热反应。正确。
考点:考查化学平衡常数的含义及浓度、温度、压强对化学平衡的影响的知识。

硫酸是一种重要的化工产品,目前主要采用“接触法”进行生产。有关接触氧化反应
2SO2 + O2 2SO3的说法中正确的是
2SO3的说法中正确的是
| A.只要选择适宜的条件,SO2和O2就能全部转化为SO3 |
| B.该反应达到平衡后,反应就完全停止了,即正逆反应速率为零 |
| C.若用18O原子组成的O2参加反应,平衡时SO2中也会含有18O |
| D.在工业合成SO3时,要同时考虑反应速率和反应能达到的限度两方面的问题 |
可逆反应mA(g)+nB(g) pC(g)+qD(g)的v-t图象如下右图,如若其它条件不变,只是在反应前加入合适的催化剂,则其v-t图象如下右图:①a1>a2②a1<a2③b1>b2④b1<b2 ⑤t1>t2 ⑥t1=t2 ⑦两图中阴影部分面积相等 ⑧右图中阴影部分面积更大,以上说法中正确的是
pC(g)+qD(g)的v-t图象如下右图,如若其它条件不变,只是在反应前加入合适的催化剂,则其v-t图象如下右图:①a1>a2②a1<a2③b1>b2④b1<b2 ⑤t1>t2 ⑥t1=t2 ⑦两图中阴影部分面积相等 ⑧右图中阴影部分面积更大,以上说法中正确的是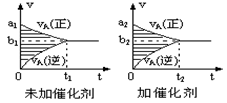
| A.②③⑤⑧ | B.①④⑥⑧ | C.②④⑤⑦ | D.①③⑥⑦ |
下列有关工业生产的叙述正确的是
| A.合成氨工业中,将NH3及时液化分离有利于加快反应速率 |
| B.氯碱工业中,使用离子交换膜可防止C12和NaOH溶液反应 |
| C.硫酸工业中,接触室内安装热交换器,是为了利用沸腾炉中排出的SO2的热量 |
| D.硫酸工业中,SO2的催化氧化不采用高压,是因为压强对SO2转化率无影响 |
在一密闭烧瓶中注入NO2,在25℃时建立下列平衡:2NO2 N2O4(正反应为放热反应),若把烧瓶置于100℃的沸水中,下列情况:①颜色,②平均相对分子质量,③质量,④压强,⑤密度。其中不变的是
N2O4(正反应为放热反应),若把烧瓶置于100℃的沸水中,下列情况:①颜色,②平均相对分子质量,③质量,④压强,⑤密度。其中不变的是
| A.②④ | B.③④ | C.③⑤ | D.①③ |
对于在恒温恒容容器中进行的反应A(g)+2B(g)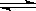 3C(g)+D(g),以下不能说明已达平衡状态的是
3C(g)+D(g),以下不能说明已达平衡状态的是
| A.反应容器中,压强不随时间改变而改变 |
| B.单位时间内生成3nmolC的同时生成nmolA |
| C.反应容器中,混合气体的平均相对分子质量不再改变 |
| D.反应容器中的气体密度不随时间变化 |
下列有关说法正确的是
| A.CaCO3(s) =CaO(s)+CO2(g)室温下不能自发进行,说明该反应的△H<0 |
| B.镀铜铁制品镀层受损后,铁制品比受损前更容易生锈 |
| C.N2(g)+3H2(g) =2NH3(g) △H<0,其他条件不变时升高温度,反应速率v(H2 )和H2的平衡转化率均增大 |
| D.水的离子积常数Kw 随着温度的升高而增大,说明水的电离是放热反应 |
一定条件下,溶液的酸碱性对TiO2光催化染料R降解反应的影响如下图所示。下列判断正确的是
| A.在0~50 min之间,pH=2和pH=7时R的降解百分率相等 |
| B.溶液酸性越强,R的降解速率越小 |
| C.R的起始浓度越小,降解速率越大 |
| D.在20~25 min之间,pH=10时R的平均降解速率为0.04 mol·L-1·min-1 |
一定温度下,反应A2(g)+B2(g)??2AB(g)达到平衡的标志是( )
| A.单位时间内生成n mol A2的同时生成n mol AB |
| B.容器内的总压强不随时间的变化而变化 |
| C.单位时间内生成2n mol AB的同时生成n mol B2 |
| D.单位时间内生成n mol A2的同时生成n mol B2 |