题目内容
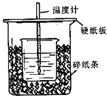 用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:(1)从实验装置上看,图中尚缺少的一种玻璃仪器是
(2)若上述HCl和NaOH溶液的密度都近似为1g/cm3,中和后生成的溶液的比热容为C(J/(g?℃),实验起始温度为t1℃,终止温度为t2℃,则该中和反应放出的热量为
(3)在实验过程中,该同学需要测定并记录的实验数据有
A.盐酸的浓度 B.盐酸的温度
C.氢氧化钠溶液的浓度 D.氢氧化钠溶液的温度
E.水的比热容 F.反应后混合溶液的终止温度
(4)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量
(5)用相同浓度和体积的氨水(NH3?H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会
考点:中和热的测定
专题:化学反应中的能量变化
分析:(1)根据量热计的构造来判断该装置的缺少仪器;
(2)反应放出的热量和所用酸以及碱的量的多少有关,并根据中和热的概念和实质来回答;
(3)根据中和热计算公式Q=cm△T中涉及的未知数据进行判断;
(4)反应放出的热量和所用酸以及碱的量的多少有关;根据中和热的概念和实质来回答;
(5)根据弱电解质电离吸收热量.
(2)反应放出的热量和所用酸以及碱的量的多少有关,并根据中和热的概念和实质来回答;
(3)根据中和热计算公式Q=cm△T中涉及的未知数据进行判断;
(4)反应放出的热量和所用酸以及碱的量的多少有关;根据中和热的概念和实质来回答;
(5)根据弱电解质电离吸收热量.
解答:
解:(1)由量热计的构造可知该装置的缺少仪器是环形玻璃搅拌棒,
故答案为:环形玻璃搅拌棒;
(2)50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行中和反应生成水的物质的量为0.05L×0.50mol=0.025mol,溶液的质量为100ml×1g/cm3=100g,温度变化的值△T为(t2-t1)℃,则生成0.025mol水放出的热量为Q=m?c?△T=100g×C(J/(g?℃)×(t2-t1)℃=100C(t2-t1)J,即0.1C(t2-t1)kJ,所以实验测得的中和热△H=-
=-4C(t2-t1)kJ/mol;
故答案为:0.1C(t2-t1);4C(t2-t1)
(3)由Q=cm△T可知,测定中和热需要测定的数据为:B.盐酸的温度、D.氢氧化钠溶液的温度、F.反应后混合溶液的终止温度:故选BDF;
(4)反应放出的热量和所用酸以及碱的量的多少有关,若用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,生成水的量增多,所放出的热量偏高,但是中和热的均是强酸和强碱反应生成1mol水时放出的热,与酸碱的用量无关,所以用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,测得中和热数值相等;
故答案为:不相等;相等;
(5)氨水为弱碱,电离过程为吸热过程,用相同浓度和体积的氨水(NH3?H2O)代替NaOH溶液进行上述实验,测得的中和热的数值偏小;
故答案为:偏小.
故答案为:环形玻璃搅拌棒;
(2)50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行中和反应生成水的物质的量为0.05L×0.50mol=0.025mol,溶液的质量为100ml×1g/cm3=100g,温度变化的值△T为(t2-t1)℃,则生成0.025mol水放出的热量为Q=m?c?△T=100g×C(J/(g?℃)×(t2-t1)℃=100C(t2-t1)J,即0.1C(t2-t1)kJ,所以实验测得的中和热△H=-
| 0.1C(t2-t1)kJ |
| 0.025mol |
故答案为:0.1C(t2-t1);4C(t2-t1)
(3)由Q=cm△T可知,测定中和热需要测定的数据为:B.盐酸的温度、D.氢氧化钠溶液的温度、F.反应后混合溶液的终止温度:故选BDF;
(4)反应放出的热量和所用酸以及碱的量的多少有关,若用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,生成水的量增多,所放出的热量偏高,但是中和热的均是强酸和强碱反应生成1mol水时放出的热,与酸碱的用量无关,所以用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,测得中和热数值相等;
故答案为:不相等;相等;
(5)氨水为弱碱,电离过程为吸热过程,用相同浓度和体积的氨水(NH3?H2O)代替NaOH溶液进行上述实验,测得的中和热的数值偏小;
故答案为:偏小.
点评:本题考查热反应热的测定与计算,题目难度大,注意理解中和热的概念以及测定反应热的原理等问题.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案
相关题目
质量相同的下列醇分别与过量的钠作用放出氢气最多的是( )
| A、甲醇 | B、乙醇 |
| C、乙二醇 | D、丙三醇 |
化学与生产、生活、科技等密切相关,下列说法正确的是( )
| A、石油裂解的目的是提高汽油等轻质油的产量和质量 |
| B、“神州七号”的防护层中含聚四氟乙烯,聚四氟乙烯属于不饱和烃 |
| C、高温能杀死流感病毒是因为构成病毒的蛋白质受热变性 |
| D、苯酚稀溶液常用于外科消毒,所以自来水也可以用苯酚进行消毒处理 |
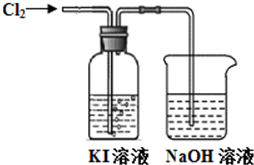 某同学对Cl2与KI溶液的反应进行了实验探究.反应装置如下:
某同学对Cl2与KI溶液的反应进行了实验探究.反应装置如下: