题目内容
根据元素周期表回答下列问题:
(1)金属性最强的元素是 ,非金属性最强的元素是 ;
(2)第3周期中,原子半径最小的元素(稀有气体元素除外)是 ,非金属性最强的元素是 ;
(3)ⅦA族中,原子半径最大的元素是 ,非金属性最弱的元素是 .
(1)金属性最强的元素是
(2)第3周期中,原子半径最小的元素(稀有气体元素除外)是
(3)ⅦA族中,原子半径最大的元素是
考点:元素周期表的结构及其应用,元素周期律的作用
专题:元素周期律与元素周期表专题
分析:(1)元素周期表左下方的金属,金属性最强;元素周期表右上方的非金属,非金属性最强(稀有气体除外);
(2)第3周期中,从左向右原子半径在减小,非金属性在增强;
(3)ⅦA族中,从上到下原子半径在增大,非金属性在减弱.
(2)第3周期中,从左向右原子半径在减小,非金属性在增强;
(3)ⅦA族中,从上到下原子半径在增大,非金属性在减弱.
解答:
解:(1)元素周期表中,金属性最强的元素是Cs;非金属性最强为F,故答案为:Cs;F;
(2)第3周期中,从左向右原子半径在减小,非金属性在增强,则第3周期中,原子半径最小的元素是Cl,非金属性最强的元素是Cl,故答案为:Cl;Cl;
(3)ⅦA族中,从上到下原子半径在增大,非金属性在减弱,则ⅦA族中,原子半径最大的元素是At,非金属性最弱的元素是At,故答案为:At;At.
(2)第3周期中,从左向右原子半径在减小,非金属性在增强,则第3周期中,原子半径最小的元素是Cl,非金属性最强的元素是Cl,故答案为:Cl;Cl;
(3)ⅦA族中,从上到下原子半径在增大,非金属性在减弱,则ⅦA族中,原子半径最大的元素是At,非金属性最弱的元素是At,故答案为:At;At.
点评:本题考查元素周期表的结构及应用,为高频考点,把握元素的金属性、非金属性比较为解答的关键,注意同主族、同周期元素性质变化规律,题目难度不大.

练习册系列答案
 初中暑期衔接系列答案
初中暑期衔接系列答案
相关题目
水溶液中能大量共存的一组离子是( )
| A、Na+、Al3+、Cl-、HCO3- |
| B、H+、Fe2+、NO3-、SO42- |
| C、H+、Mg2+、Cl-、NO3- |
| D、K+、Ag+、OH-、SO42- |
关于氮的变化关系图如下:
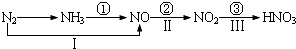
则下列说法正确的是( )

则下列说法正确的是( )
| A、路线①②③是工业生产硝酸的主要途径 |
| B、路线ⅠⅡⅢ是雷电固氮生成硝酸的主要途径 |
| C、上述并不是所有反应都是氧化还原反应 |
| D、上述反应中①②③均属于氮的固定 |
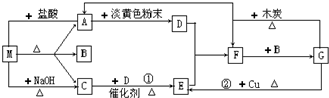
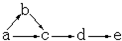 a、b、c、d、e是含有一种相同元素的五种物质,可发生如下转化:
a、b、c、d、e是含有一种相同元素的五种物质,可发生如下转化: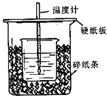 用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: