题目内容
下列变化的离子方程式书写正确的是( )
| A、将少量AgNO3溶液滴入氨水中:Ag++2NH3?H2O═[Ag(NH3)2]++2H2O |
| B、将少量SO2通入NaClO溶液中:SO2+2ClO-+H2O═SO32-+2HClO |
| C、澄清石灰水与稀硝酸反应:Ca(OH)2+2H+═2H2O+Ca2+ |
| D、水玻璃长时间放置在空气中:SiO32-+CO2═H2SiO3↓+HCO3- |
考点:离子方程式的书写
专题:离子反应专题
分析:A.银离子与过量氨水反应生成银铵络离子;
B.次氯酸具有强氧化性,能够将亚硫酸根离子氧化成硫酸根离子;
C.澄清石灰水中,氢氧化钙不能写成化学式,应该拆开写成离子形式;
D.根据电荷守恒、质量守恒定律进行判断,离子方程式两边电荷、质量都不守恒.
B.次氯酸具有强氧化性,能够将亚硫酸根离子氧化成硫酸根离子;
C.澄清石灰水中,氢氧化钙不能写成化学式,应该拆开写成离子形式;
D.根据电荷守恒、质量守恒定律进行判断,离子方程式两边电荷、质量都不守恒.
解答:
解:A.少量AgNO3溶液滴入氨水中,反应生成银铵络离子,反应的离子方程式为:Ag++2NH3?H2O═[Ag(NH3)2]++2H2O,故A正确;
B.少量SO2通入NaClO溶液中,次氯酸将二氧化硫氧化成硫酸根离子,正确的离子方程式为:ClO-+H2O+SO2═SO42-+2H++Cl-,故B错误;
C.澄清石灰水与稀硝酸反应,反应的实质为氢离子与氢氧根离子反应生成水,正确的离子方程式为:OH-+H+═H2O,故C错误;
D.水玻璃长时间放置在空气中,反应生成硅酸沉淀和 碳酸氢根离子,正确的离子反应为:SiO32-+2CO2+2H2O═H2SiO3↓+2HCO3-,故D错误;
故选A.
B.少量SO2通入NaClO溶液中,次氯酸将二氧化硫氧化成硫酸根离子,正确的离子方程式为:ClO-+H2O+SO2═SO42-+2H++Cl-,故B错误;
C.澄清石灰水与稀硝酸反应,反应的实质为氢离子与氢氧根离子反应生成水,正确的离子方程式为:OH-+H+═H2O,故C错误;
D.水玻璃长时间放置在空气中,反应生成硅酸沉淀和 碳酸氢根离子,正确的离子反应为:SiO32-+2CO2+2H2O═H2SiO3↓+2HCO3-,故D错误;
故选A.
点评:本题考查了离子方程式的正误判断,为高考中的高频题,属于中等难度的试题,注意明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等.

练习册系列答案
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案
相关题目
1L的密闭容器中有0.3mol A、0.1mol C和一定量B三种气体.一定条件下发生反应,各物质浓度随时间变化如图甲所示,t1时刻c(B)=0.1mol/L.图乙为t2时刻后改变条件反应速率随时间的变化情况,每次改变一种条件且条件各不相同,已知,t3时刻为加入催化剂,则下列判断正确的是( )
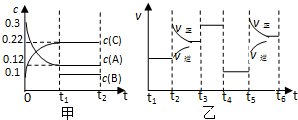

| A、t4时刻是增大容器的体积 |
| B、B的起始浓度为0.06mol/L |
| C、t1、t3、t6时刻相比,A物质的量最大的是t6时刻 |
| D、该可逆反应的方程式为:3A(g)?B(g)+2C(g) |
下列关于有机化合物的认识正确的是( )
| A、天然油脂是高分子化合物,同时也是混合物 |
| B、淀粉、纤维素的分子式都是(C6H10O5)n,二者互为同分异构体 |
| C、氨基酸和蛋白质分子中都含有氨基和羧基,二者均有两性 |
| D、糖类、油脂、蛋白质均能发生水解 |
用NA表示阿伏伽德罗常数.下列说法正确的是( )
| A、标准状况下,11.2L乙烯含有的极性共价键数为NA |
| B、常温下,5.6LNO和5.6LO2的混合气体中含有的分子数为0.5NA |
| C、16.9gBaO2固体中阴、阳离子总数为0.2NA |
| D、含有1molFe(OH)3的氢氧化铁胶体中含有胶粒数为NA |
下列有机物的工业制法错误的是( )
| A、乙烯氧化法制乙醛 |
| B、无水醋酸钠与碱石灰共热制甲烷 |
| C、石油裂化制汽油 |
| D、煤干馏制苯酚 |
下列与有机物的结构、性质、用途有关的叙述,不正确的是( )
| A、乙醇、乙酸、乙酸乙酯都能发生取代反应 |
| B、乙酸乙酯、油脂与NaOH溶液反应均有醇生成 |
| C、乙烯和聚乙烯中均含有不饱和碳碳双键 |
| D、淀粉和蛋白质都是高分子化合物 |
某有机物的结构为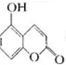 ,下列有关说法正确的是( )
,下列有关说法正确的是( )
 ,下列有关说法正确的是( )
,下列有关说法正确的是( )| A、1mol该物质与足量浓溴水反应,最多消耗2mol Br2 |
| B、1mol该物质最多能与2mol NaOH反应 |
| C、1mol该物质最多能与3mol H2加成 |
| D、该物质的核磁共振氢谱共有6个吸收峰 |
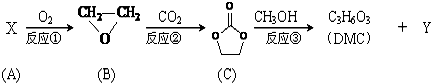
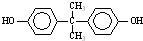 )在一定条件下发生缩聚反应,可生成芳香族聚碳酸酯,写出反应的化学方程式
)在一定条件下发生缩聚反应,可生成芳香族聚碳酸酯,写出反应的化学方程式
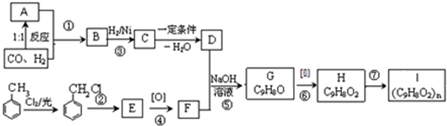
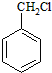 为主要原料合成
为主要原料合成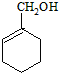 ,请设计四步合成路线(无机试剂及溶剂任选).
,请设计四步合成路线(无机试剂及溶剂任选).