题目内容
(1)按要求写出下列各类具体反应的例子:
①两种弱酸相互反应生成两种强酸: 。
②两种弱酸盐相互反应生成两种强酸盐: 。
③两种酸溶液相互反应后溶液酸性减弱: 。
④一种酸与一种盐溶液反应后溶液酸性增强。 。
(2)广西盛产重晶石矿,其主要成分是 ;以BaSO4为原料通过如下反应可制得BaS:
BaSO4+4C ![]() BaS+4CO↑
BaS+4CO↑
①上述反应中, 元素被氧化, 是氧化剂。
②BaS与盐酸反应可制得BaCl2,在此过程中会产生污染环境的物质,消除污染的方法是 ,有关的化学反应方程式是 。
(1)①H2SO3+HClO ![]() H2SO4+HCl
H2SO4+HCl
②Na2SO3+NaClO ![]() Na2SO4+NaCl
Na2SO4+NaCl
③H2SO3+2H2S ![]() 3S↓+3H2O
3S↓+3H2O
④H2S+CuSO4 ![]() CuS↓+H2SO4
CuS↓+H2SO4
(2)BaSO4 ①碳 硫酸钡 ②将产生的气体通入NaOH溶液中 H2S+2NaOH ![]() Na2S+2H2O
Na2S+2H2O
解析:
(1)按题目要求,选择合适的反应物并写出化学方程式,如:①H2SO3与HClO;?②Na2SO3?与?NaClO;?③H2SO3与H2S;④H2S与CuSO4。
(2)重晶石的主要成分为BaSO4;①分析所给氧化还原反应中有关元素化合价的变化可知:BaSO4中+6价的硫变为BaS中的-2价,被还原;而单质碳由0价变为CO中的+2价,被氧化;②BaS与盐酸反应制得BaCl2的同时,会产生污染环境的H2S气体,可以用NaOH溶液吸收。

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案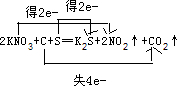
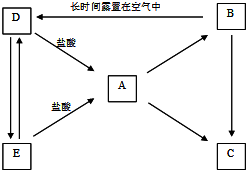 A、B、C、D、E五种物质的焰色反应都显黄色,电解熔融的A可以得到单质B,电解A的水溶液可以得到碱性溶液C.转化关系如图:
A、B、C、D、E五种物质的焰色反应都显黄色,电解熔融的A可以得到单质B,电解A的水溶液可以得到碱性溶液C.转化关系如图: