题目内容
同时向五个温度不同、容积相同的恒容密闭容器中,分别加入等量的原料气(SO2和O2),发生反应:2SO2(g)+O2(g)?2SO3(g)△H<0.经过相同的反应时间后,分别测定五个容器中SO2的转化率(α),并作出其随反应温度(T)变化的关系图.下列示意图中,不可能与实验结果相符的是( )
A、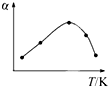 |
B、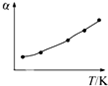 |
C、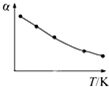 |
D、 |
考点:化学平衡的影响因素
专题:图示题,化学平衡专题
分析:发生反应:2SO2(g)+O2(g)?2SO3(g)△H<0.反应是气体体积减小的放热反应,升温平衡逆向进行,结合反应过程分析,开始反应正向进行,二氧化硫转化率增大,平衡后升温平衡逆向进行,二氧化硫转化率减小.
解答:
解:结合反应过程分析,开始反应正向进行,二氧化硫转化率增大,平衡后升温平衡逆向进行,二氧化硫转化率减小;
A、图象中随温度升高,二氧化硫转化率增大后减小,可能是费用开始二氧化硫转化率增大,达到平衡状态,升温平衡逆向进行,转化率减小,故A可能;
B、图象中随温度升高,二氧化硫转化率增大,可能是开始反应阶段,二氧化硫随反应进行增大,故B可能;
C、图象中随温度升高,二氧化硫转化率减小,可能是平衡状态升温,平衡逆向进行,二氧化硫转化率减小,故C可能;
D、图象中二氧化硫随温度升高减小可能是破坏状态升温平衡逆向进行,后增大不可能,故D不可能;
故选D.
A、图象中随温度升高,二氧化硫转化率增大后减小,可能是费用开始二氧化硫转化率增大,达到平衡状态,升温平衡逆向进行,转化率减小,故A可能;
B、图象中随温度升高,二氧化硫转化率增大,可能是开始反应阶段,二氧化硫随反应进行增大,故B可能;
C、图象中随温度升高,二氧化硫转化率减小,可能是平衡状态升温,平衡逆向进行,二氧化硫转化率减小,故C可能;
D、图象中二氧化硫随温度升高减小可能是破坏状态升温平衡逆向进行,后增大不可能,故D不可能;
故选D.
点评:本题考查了图象分析判断,化学平衡移动原理的分析应用是关键,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
某单质能与足量的浓HNO3反应放出NO2气体,若参加反应的单质和硝酸的物质的量之比为1:a,则该元素在反应中所显示的化合价是( )
| A、+2a | ||
| B、+a | ||
C、+
| ||
D、+
|
已知有如下反应,对下列氧化性和还原性的强弱判断正确的是( )
①2Fe3++2I-═2Fe2++I2
②2Fe2++Br2═2Fe3++2Br-
③2Fe(CN)64-+I2═2Fe(CN)63-+2I-.
①2Fe3++2I-═2Fe2++I2
②2Fe2++Br2═2Fe3++2Br-
③2Fe(CN)64-+I2═2Fe(CN)63-+2I-.
| A、氧化性:Fe3+>Br2>I2>Fe(CN)63- |
| B、还原性:Fe(CN)64->I->Fe2+>Br- |
| C、氧化性:Br2>Fe3+>I2>Fe(CN)63- |
| D、还原性:Fe(CN)64->Fe2+>I->Br- |
一定条件下,通过下列反应可实现燃煤烟气中的硫的回收:SO2(g)+2CO(g)?2CO2(g)+S(l)△H<0
一定温度下,在容积为2L的恒容密闭容器中充入1mol SO2和n mol CO发生反应,5min后达到平衡,生成2a mol CO2.下列说法正确的是( )
一定温度下,在容积为2L的恒容密闭容器中充入1mol SO2和n mol CO发生反应,5min后达到平衡,生成2a mol CO2.下列说法正确的是( )
| A、平衡后保持其它条件不变,从容器中分离出部分硫,平衡向正反应方向移动 |
| B、当混合气体的物质的量不再改变时,反应达到平衡状态 |
| C、平衡后保持其它条件不变,升高温度和加入催化剂,SO2的转化率均增大 |
| D、反应前2min的平均速率v(SO2)=0.1a mol/(L?min) |
下列说法不正确的是( )
| A、金属氧化物都是碱性氧化物 |
| B、盐电离出的离子一定有金属离子 |
| C、由同种元素组成的物质一定是单质 |
| D、非金属氧化物都是酸性氧化物 |
能正确表示下列化学反应的离子方程式的是( )
| A、碳酸钙溶于稀盐酸中:CO32-+2H+=H2O+CO2↑ |
| B、澄清的石灰水与稀盐酸反应:Ca(OH)2+2H+=Ca2++2H2O |
| C、铜片插入硝酸银溶液中:Cu+Ag+=Cu2++Ag |
| D、氢氧化钡溶液与盐酸的反应:OH-+H+=H2O |
下列离子方程式中,正确的是( )
| A、石灰石与醋酸反应:CaCO3+2H+=Ca2++CO2↑+H2O |
| B、氧化铁和稀硫酸反应:O2-+2H+=H2O |
| C、向NaHSO4溶液中加入过量的Ba(OH)2溶液:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| D、向NaHCO3溶液中加入过量的Ba(OH)2溶液:Ba2++OH-+H++CO32-=BaCO3↓+H2O |
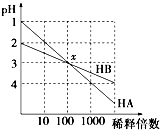 HA和HB两种酸的溶液分别加水稀释时,pH变化的简图如图所示,下列叙述中不正确的是( )
HA和HB两种酸的溶液分别加水稀释时,pH变化的简图如图所示,下列叙述中不正确的是( )| A、HA是一种强酸 |
| B、x点,[A-]=[B-] |
| C、HB是一种弱酸 |
| D、原溶液中HA的物质的量浓度为HB的10倍 |