��Ŀ����
����Ŀ����ͼ����ʵ���ҽ��ж��������Ʊ�������ʵ������װ�ã��ص��������⣺
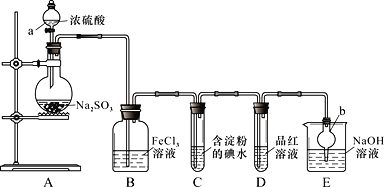
��1���������ƣ�a_____��b_____��װ��A����ȡSO2ʱ������ϡH2SO4����ŨH2SO4��ԭ����________________________��
��2��Ϊ����֤B�з�����������ԭ��Ӧ��Ӧ��B�м��������Լ��е�______������ţ���
��KMnO4��Һ ��ϡ�����ữ��BaCl2��Һ ��NaOH��Һ ��KSCN��Һ
��˵��I����ԭ������SO2������Ϊ________��������Ӧ�����ӷ���ʽ��_______��
��3��Ҫ��֤SO2��Ʒ�췴Ӧ�IJ��ﲻ�ȶ���ʵ�����������������_______________��ʵ���е�β����NaOH��Һ���գ���Ӧ�����ӷ���ʽ��_______________��
��4��ͭ��Ũ�����ڼ��������·�ӦҲ����SO2���÷�Ӧ������ŨH2SO4����Щ���ʣ�________����Ӧ�Ļ�ѧ����ʽ��_______________��
���𰸡� ��Һ©�� ����� SO2��ˮ�е��ܽ�Ƚϴ���ϡH2SO4������SO2���ݳ� �� C�Թ�����Һ��ɫ��ȥ SO2��I2��2H2O==2I����SO![]() ��4H�� �þƾ��ƶ�D�Թ���Һ��������Һ�ָ�Ϊ��ɫ SO2��2OH��==SO
��4H�� �þƾ��ƶ�D�Թ���Һ��������Һ�ָ�Ϊ��ɫ SO2��2OH��==SO![]() ��H2O ǿ�����ԡ����� Cu��2H2SO4(Ũ)
��H2O ǿ�����ԡ����� Cu��2H2SO4(Ũ)![]() CuSO4��SO2����2H2O
CuSO4��SO2����2H2O
��������(1). �������ƣ�a ��Һ©����b ����ܣ���Ӧ���ɵ�SO2������ˮ��ʹ��ϡH2SO4����������ˮ�������������ݳ���
(2). ��KMnO4��Һ���������ԣ������ã���ϡ�����ữ��BaCl2��Һ��������BaSO4��������ǿ��������ԭ�����������������������ᣬ���Կ�֤��������������ԭ��Ӧ��������������ʹ��Һ��ɫ�仯�����ԣ�NaOH��Һ�����ã���ֻҪ��Һ�к��������ӣ���Һ������Ѫ��ɫ������ȷ��Ӧ������KSCN��Һ�����á���ѡ��ڣ�C�Թ�����ɫ��ȥ��˵����������͵ⵥ�ʷ�Ӧ������I��������������ԭ��Ӧ�л�ԭ���Ļ�ԭ�Դ��ڻ�ԭ�����������ԭ�Դ��ڵ����ӣ���Ӧ�����ӷ���ʽ��SO2��I2��2H2O==2I����SO![]() ��4H����
��4H����
(3). SO2��Ʒ�췴Ӧ�IJ������Ⱦͷֽ⣬�þƾ��ƶ�D�Թ���Һ���ȣ���Һ�ָ�Ϊ��ɫ��˵�����ﲻ�ȶ���ʹ��NaOH����SO2�����ӷ�Ӧ����ʽΪ��SO2��2OH��==SO![]() ��H2O��
��H2O��
(4). Ũ����ɽ�ͭ���������������壬������Ũ�����ǿ�����Ժ����ԣ���Ӧ�ڼ��������½��У���ѧ����ʽ��Cu��2H2SO4(Ũ)![]() CuSO4��SO2����2H2O��
CuSO4��SO2����2H2O��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ������ˮ��ɽ���ǽ�ɽ��ɽ����������,��ɫ��չ����̬������Ϊ�й�չʾ�������һ���¡���Ƭ��������β������ɴ�����Ⱦ����Ҫԭ��֮һ,���ٵ����������ڴ����е��ŷ��ǻ�����������Ҫ����֮һ����ش��������⣺
(1)��֪��N2(g)+O2(g)=2NO(g)��H1=+180.5kJ/mol
C(s)+O2(g)=CO2(g)��H2=-393.5kJ/mol
2C(s)+O2(g)=2CO(g)��H3=-221kJ/mol
��ij��Ӧ��ƽ�ⳣ������ʽΪ��K=[c(N2) ��c2(CO2)]/[c2(NO) ��c2(CO)],��˷�Ӧ���Ȼ�ѧ����ʽΪ____________________________________��
(2)N2O5��һ�������¿ɷ����ֽ⣺2N2O5(g)![]() 4NO2(g)+O2(g),ij�¶��º����ܱ������м���һ����N2O5,���N2O5Ũ����ʱ��ı仯���±���
4NO2(g)+O2(g),ij�¶��º����ܱ������м���һ����N2O5,���N2O5Ũ����ʱ��ı仯���±���
t/min | 0 | 1 | 2 | 3 | 4 | 5 |
c(N2O5)/<mol��L-1) | 1.00 | 0.71 | 0.50 | 0.35 | 0.25 | 0.17 |
�ٷ�Ӧ��ʼʱ��ϵѹǿΪp0,��2minʱ��ϵѹǿΪp1����p1��p0=__________��2~5min����NO2��ʾ�ĸ÷�Ӧ��ƽ����Ӧ����Ϊ__________��
��һ���¶��£��ں����ܱ������г���һ����N2O5���и÷�Ӧ,���жϷ�Ӧ�Ѵﵽ��ѧƽ��״̬����__________��(����ĸ)��
a��NO2��O2��Ũ�ȱȱ��ֲ��� b��������ѹǿ���ٱ仯
c��2v��(NO2)=v��(N2O5) d��������ܶȱ��ֲ���
(3)Kp���÷�Ӧ��ϵ���������ʵķ�ѹ����ʾ��ƽ�ⳣ��������K����ʽ��ƽ��Ũ����ƽ���ѹ���档��֪��Ӧ��NO2(g)+CO(g)![]() NO(g)+CO2(g),�÷�Ӧ������Ӧ����v��=k����p(NO2)��p(CO),�淴Ӧ����v��=k����p(NO)��p(CO2),����k����k��Ϊ���ʳ���,��KpΪ__________(��k����k����ʾ)��
NO(g)+CO2(g),�÷�Ӧ������Ӧ����v��=k����p(NO2)��p(CO),�淴Ӧ����v��=k����p(NO)��p(CO2),����k����k��Ϊ���ʳ���,��KpΪ__________(��k����k����ʾ)��
(4)��ͼ���ܱշ�Ӧ���а�n(N2) ��n(H2)=1��3Ͷ�Ϻ�,��200�桢400�桢600����,�ϳ�NH3��Ӧ�ﵽƽ��ʱ,�������NH3�����ʵ���������ѹǿ�ı仯���ߣ���֪�÷�ӦΪ���ȷ�Ӧ��
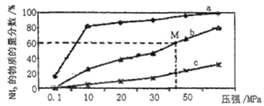
������a��Ӧ���¶���__________��
��M���Ӧ��H2��ת������__________��
(5)��ҵ�ϳ��ð�ˮ���ն�������,������(NH4)2SO3���жϳ�����(NH4)2SO3��Һ������Բ�˵���ж����ݣ�______________________________________________��(��֪��NH3��H2O��Kb=1.8��10-5;H2SO3��Ka1=1.3��10-2,Ka2=6.3��10-8��)
����Ŀ���о�С��������±���ʾ��ԭ���ʵ��:
ʵ���� | �� | �� |
ʵ��װ�� |
|
|
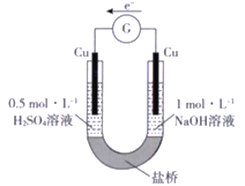
ʵ������ | ����װ��5 ���Ӻ�����������ָ������ƫת������ͭƬ��������������� | �����Ƭ��������������ݣ�����װ��5 ���Ӻ�����������ָ������ƫת���Ҳ���Ƭ�������������� |
���й��ڸ�ʵ��������У���ȷ����
A. ��װ�õ������У������Ӿ����Ҳ��ƶ�
B. ʵ�����У�����ͭ����ʴ
C. ʵ�����У����缫�ĵ缫��ӦʽΪ2H++ 2e-=H2��
D. ʵ���� ��ʵ�����У�����O2 �õ��ӵķ�Ӧ����