题目内容
4. 某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,回答下列问题:
某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,回答下列问题:(1)该反的化学反应方程式为X+3Y?2Z
(2)从开始至2min,Z的平均反应速率是0.05mol•(L•min)-1;
(3)第4分钟时下列叙述正确的是BD;
A.该反应已停止
B. 该反应为可逆反应
C.3v(X)=2v(Z)
D.c(X):c(Y):c(Z)=7:9:2.
分析 (1)根据物质的量的变化判断反应物和生成物,根据物质的量的变化之比等于化学计量数之比书写方程式;
(2)根据v=$\frac{△c}{△t}$计算反应速率;
(3)根据第4分钟时,各物质的量不变,则反应达平衡状态,反应速率之比等于系数之比,据此分析解答.
解答 解:(1)由图象可以看出,反应中X、Y的物质的量减小,Z的物质的量增多,则X、Y为反应物,Z为生成物,且△n(X):△n(Y):△n(Z)=0.1mol:0.3mol:0.2mol=1:3:2,则反应的化学方程式为:X+3Y?2Z,
故答案为:X+3Y?2Z;
(2)v(Z)=$\frac{\frac{0.2mol}{2L}}{2min}$=0.05mol•(L•min)-1,故答案为:0.05mol•(L•min)-1;
(3)由图象可知,第4分钟时,各物质的量不变并且反应物不为0,说明反应达平衡状态,则
A.该反应为动态平衡,反应不会停止,故A错误;
B. 该反应为可逆反应,故B正确;
C.反应速率之比等于系数之比,所以2v(X)=v(Z),则C错误;
D.根据平衡时X、Y、Z的量得出c(X):c(Y):c(Z)=7:9:2,故D正确;
故选:BD.
点评 本题考查化学平衡图象分析题目,题目难度不大,注意分析各物质的量的变化曲线,把握化学方程式的判断方法.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
14.下列物质的熔沸点比较错误的是( )
| A. | NH3>PH3 | B. | CO2>SiO2 | C. | SiCl4>CCl4 | D. | MgO>KCl |
15.羟基扁桃酸可由苯酚和乙醛酸通过一步反应制得,下列有关说法正确的是( )
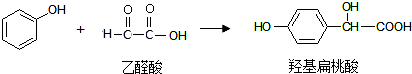

| A. | 羟基扁桃酸可以发生加成反应 | |
| B. | 上述反应属于取代反应 | |
| C. | 乙醛酸的核磁共振氢谱中有2个吸收峰 | |
| D. | 羟基扁桃酸能发生消去反应 |
12.下列物质中,既有离子键,又有非极性共价键的是( )
| A. | H2SO4 | B. | CaCl2 | C. | NH4Cl | D. | Na2O2 |
19.下列过程中,离子键被破坏的是( )
| A. | 干冰升华 | B. | KNO3熔化 | C. | NaCl溶于水 | D. | HCl气体溶于水 |
16. 现用中和滴定法测定某盐酸溶液的浓度,有关数据记录如下:
现用中和滴定法测定某盐酸溶液的浓度,有关数据记录如下:
(1)滴定管如图所示,用乙滴定管盛装0.2500mol/L氢氧化钠标准液 (填“甲”或“乙”).根据所给数据,该盐酸溶液的浓度为0.2632 mol/L
(2)现实验室中有石蕊和酚酞两种指示剂,该实验应选酚酞作指示剂,判断滴定终点的现象是滴入最后一滴标准液,溶液由无色变成浅红色,且半分钟内不恢复原来的颜色
(3)下列操作会使所测得的盐酸的浓度偏低的是D.
A.盛装待测液的锥形瓶用水洗后未干燥
B.滴定前,碱式滴定管尖端有气泡,滴定后气泡消失
C.碱式滴定管用蒸馏水洗净后,未用标准氢氧化钠溶液润洗
D.读碱式滴定管的刻度时,滴定前仰视凹液面最低处,滴定后俯视读数.
 现用中和滴定法测定某盐酸溶液的浓度,有关数据记录如下:
现用中和滴定法测定某盐酸溶液的浓度,有关数据记录如下:| 实验编号 | 待测液体积/mL | 所消耗氢氧化钠标准液的体积/mL |
| 1 | 25.00 | 26.30 |
| 2 | 25.00 | 26.34 |
| 3 | 25.00 | 19.36 |
(2)现实验室中有石蕊和酚酞两种指示剂,该实验应选酚酞作指示剂,判断滴定终点的现象是滴入最后一滴标准液,溶液由无色变成浅红色,且半分钟内不恢复原来的颜色
(3)下列操作会使所测得的盐酸的浓度偏低的是D.
A.盛装待测液的锥形瓶用水洗后未干燥
B.滴定前,碱式滴定管尖端有气泡,滴定后气泡消失
C.碱式滴定管用蒸馏水洗净后,未用标准氢氧化钠溶液润洗
D.读碱式滴定管的刻度时,滴定前仰视凹液面最低处,滴定后俯视读数.
13.下列说法中,不正确的是( )
| A. | 硫既可做氧化剂,又可做还原剂 | B. | SO3只有氧化性 | ||
| C. | 可以用铁罐贮运冷的浓H2SO4 | D. | H2S既有氧化性又有还原性 |
14.除去下列物质中含有的少量杂质,请选择合适的所给试剂、操作方法填入下表中(只填序号)
试剂:A.溴水 B.NaOH溶液 C.CaO D.酸性KMnO4 溶液 E.饱和Na2CO3溶液
操作方法:a.蒸馏 b.分液 c.洗气 d.过滤 e.干馏 f.分馏 g.裂化
试剂:A.溴水 B.NaOH溶液 C.CaO D.酸性KMnO4 溶液 E.饱和Na2CO3溶液
操作方法:a.蒸馏 b.分液 c.洗气 d.过滤 e.干馏 f.分馏 g.裂化
| 组别 | 物质 | 杂质 | 试剂 | 操作方法 |
| 1 | 乙烷 | 乙烯 | ||
| 2 | 溴苯 | 溴 | ||
| 3 | 乙酸乙酯 | 乙酸 | ||
| 4 | 乙醇 | 水 | ||
| 5 | 将重油转化为汽油 | |||
| 6 | 把煤转化为焦炉气、煤焦油和焦炭等 | |||
