题目内容
19.下列过程中,离子键被破坏的是( )| A. | 干冰升华 | B. | KNO3熔化 | C. | NaCl溶于水 | D. | HCl气体溶于水 |
分析 活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,离子键被破坏可能发生化学反应,也可能发生离子化合物的电离.
解答 解:A.干冰是分子晶体,升华时只是状态发生变化,破坏分子间作用力,故A错误;
B.硝酸钾熔化时电离出阴阳离子而破坏离子键,故B正确;
C.NaCl在水分子的作用下电离出自由移动的钠离子、氯离子,所以离子键被破坏,故C正确;
D.HCl溶于水时,在水分子的作用下电离出自由移动的氯离子和氢离子,共价键被破坏,故D错误;
故选BC.
点评 本题考查离子键和共价键,侧重考查基本概念,明确离子键和共价键的区别即可解答,注意有化学键断裂不一定有化学键形成,为易错点.

练习册系列答案
相关题目
9.欲除去下列物质中混入的少量杂质(括号内物质为杂质),不能达到目的是( )
| A. | 乙酸乙酯(乙酸):加饱和碳酸钠溶液,充分振荡静置后,分液 | |
| B. | 乙醇(水):加入新制生石灰,蒸馏 | |
| C. | 溴苯(溴):加入CCl4溶液,充分振荡静置后,分液 | |
| D. | 苯中混有苯酚,加入氢氧化钠溶液,再用分液漏斗分液 |
10.R、W、X、Y、Z是同一短周期主族元素,原子序数依次递增.下列说法一定正确的是(m,n均为整数)( )
| A. | 若R(OH)n为强碱,则W(OH)m也为强碱 | |
| B. | 若Y的最低负化合价为-2,则Z的最高正化合价为+6 | |
| C. | 若HnXOm为强酸,则Y是活泼非金属元素 | |
| D. | 若X的最高正化合价为+5,则五种元素一定都是非金属元素 |
7.设NA表示阿伏加德罗常数,下列说法不正确的是( )
| A. | 1mol氯气参加氧化还原反应,转移的电子数一定为2 NA | |
| B. | 0.1mol Fe与0.1mol Cl2充分反应,转移的电子数为0.3NA | |
| C. | 常温常压下,44g二氧化碳分子中所形成的共用电子对数为4NA | |
| D. | 常温常压下,1.6gO2和O3混合气体中质子总数为0.8NA |
11.下列用电子式表示物质的形成过程中正确的是( )
| A. | Na•+Cl:→[Na]+[•Cl:]- | B. | H2•+•O•→H:O:H | ||
| C. | 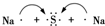 →Na+[${\;}_{•}^{•}$$\underset{\stackrel{••}{S}}{••}$${\;}_{•}^{•}$]2-Na+ →Na+[${\;}_{•}^{•}$$\underset{\stackrel{••}{S}}{••}$${\;}_{•}^{•}$]2-Na+ | D. |  →H:F →H:F |
8.设阿伏加德罗常数的值为NA,下列说法中正确的是( )
| A. | 1mol苯乙烯中含有的C=C数为4NA | |
| B. | 1mol甲醇中含有C-H键的数目为4NA | |
| C. | 0.1molCnH2n+2中含有的C-C键数为0.1NA | |
| D. | 1molC4H10中含有共用电子对数是13NA |
9.加热的条件下,铝与下列溶液作用产生H2的是( )
| A. | 浓硫酸 | B. | 浓硝酸 | C. | 稀硝酸 | D. | NaOH溶液 |

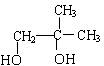 ;
;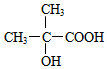 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$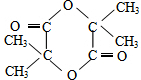 +2H2O.
+2H2O.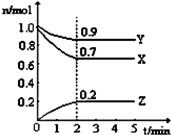 某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,回答下列问题:
某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,回答下列问题: