题目内容
17.实验室制备Cl2的过程中有水蒸气和HCl挥发,甲同学设计如图装置进行验证,请回答下列问题.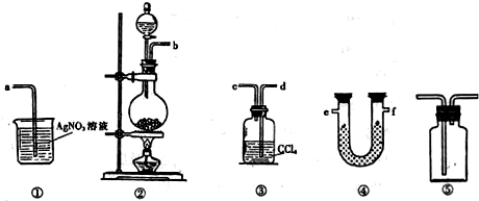
(1)写出装置②中反应化学方程式MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,为减少HCl挥发应采取的操作措施为逐滴加入浓盐酸,缓慢加热
(2)请根据甲同学的意图,连接相应的装置,接口的顺序:b接e,f接d,c接a,U形管中所盛试剂的化学式为无水CuSO4,装置③中CCl4的作用是吸收Cl2.
(3)乙同学认为甲同学实验不能证明最终通入AgNO3溶液中额气体只有HCl.为确保实验结论的可靠性,乙同学提出在某两个装置之间加装置⑤,则装置⑤应加在③①之间(按连接顺序填装置序号),瓶中可以放入湿润的淀粉KI试纸(或湿润的有色布条)进行检验.
(4)丙同学认为只需将原来烧杯中的AgNO3溶液换成紫色石蕊试液溶液,如果观察到紫色石蕊试液变红色而不褪色现象,则证明Cl2时有HCl挥发.
分析 (1)装置②中是二氧化锰和浓盐酸发生反应生成氯化锰、氯气和水,减缓氯化氢挥发可以逐滴滴入,缓慢加热等;
(2)根据实验原理和目的及各装置的作用决定仪器排列组装顺序,U形管中所盛试剂作用是检验水蒸气的存在,实验室常用无水硫酸铜检验水的存在,装置③除去氯气,防止HCl干扰检验;
(3)①装置用来检验HCl气体,为了确保实验结论的可靠性,应排除氯气的干扰,故应检验氯气是否除尽,检验氯气通常用湿润的KI淀粉试纸(或湿润的有色布条);
(4)HCl呈酸性,使紫色石蕊试液变红,Cl2使紫色石蕊试液先变红后褪色.
解答 解:(1)装置②中是二氧化锰和浓盐酸发生反应生成氯化锰、氯气和水,反应的化学方程式为:反应的化学方程式为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,为减少HCl挥发应采取的操作措施逐滴加入,缓慢加热减少氯化氢挥发,
故答案为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;逐滴滴入浓盐酸,缓慢加热等;
(2)先验证制备的氯气中是否含有水蒸气,然后除去氯气,再检验是否含有氯化氢,所以相应的装置接口连接顺序为b,e,f,d,c,a,无水硫酸铜与水反应生成蓝色五水硫酸铜晶体,可用来检验水,氯气易溶于四氯化碳溶液,可用来吸收氯气,防止HCl干扰检验,
故答案为:e;f;d;c;无水CuSO4;吸收氯气;
(3)①装置用来检验HCl气体,为了确保实验结论的可靠性,应排除氯气的干扰,在③吸收氯气之后要检验氯气是否完全除去,根据氯气具有强氧化性的性质,可用湿润的淀粉KI试纸检验,如不变色,说明已经完全除去,
故答案为:①③;湿润的淀粉KI试纸(或湿润的有色布条);
(4)HCl呈酸性,使紫色石蕊试液变红,Cl2使紫色石蕊试液先变红后褪色.若只变红不褪色,说明制Cl2时有HCl挥发出来.
故答案为:紫色石蕊试液; 紫色石蕊溶液变红且不褪色.
点评 本题以氯气的制备和性质的检验为载体,考查学生对实验方案设计评价,题目综合性较强合,难度中等.关键理清实验原理和目的及各装置的作用.

| A. | 加水,将湿润的红色石蕊试纸放在试管口 | |
| B. | 加氢氧化钠溶液,加热,滴入紫色石蕊试剂 | |
| C. | 加氢氧化钠溶液,加热,滴入酚酞试剂 | |
| D. | 加氢氧化钠溶液,加热,将湿润的红色石蕊试纸放在试管口 |
| A. | 过氧化氢有“绿色氧化剂”之称,故过氧化氢只能作氧化剂 | |
| B. | 氯气常用于自来水的杀菌消毒,其中起杀菌消毒作用的是氯气 | |
| C. | 过氧乙酸(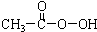 )分子中既有极性键又有非极性键 )分子中既有极性键又有非极性键 | |
| D. | 4.8g臭氧与3.36L氧气含有的原子总数相等 |
Ⅰ、向粗盐水中加入过量BaCl2溶液,操作X;
Ⅱ、向所得滤液中加入过量Na2CO3溶液,过滤;
Ⅲ、滤液用盐酸调节pH,获得第一次精制盐水.
(1)操作X使用的主要仪器为:漏斗、烧杯、玻璃棒.
(2)过程Ⅰ、Ⅱ生成的部分沉淀及其溶解度(20℃/g)如下表,请依据表中数据解释下列问题:
| CaSO4 | Mg2(OH)2CO3 | CaCO3 | BaSO4 | BaCO3 |
| 2.6×10-2 | 2.5×10-4 | 7.8×10-4 | 2.4×10-4 | 1.7×10-3 |
②过程Ⅱ之后检测Ca2+、Mg2+及过量Ba2+是否除尽时,只需检测Ba2+即可,检验Ba2+的操作是取少量清液放置于试管中,先加入盐酸,再加入硫酸钠溶液,若无白色沉淀,则可证明溶液无Ba2+.
(3)第二次精制要除去微量的I-、IO3-、NH4+、Ca2+、Mg2+,流程示意如下:

①过程Ⅳ除去NH4+的离子方程式是3ClO-+2NH4+=3Cl-+N2↑+2H++3H2O.
②实验室从水溶液分离出I2的操作名称为萃取.
③过程Ⅵ中,产品NaOH在电解槽的阴极区生成(填“阳极”或“阴极”),该电解槽为阳离子交换膜电解槽(填“阳”或“阴”).
| A. | 神舟飞船所用太阳能电池板可将光能转换为电能,所用转换材料是单晶硅 | |
| B. | 二氧化氯具有还原性,可用于自来水的杀菌消毒 | |
| C. | 乙醇和汽油都是可再生能源,应大力推广使用乙醇汽油 | |
| D. | “辽宁舰”上用于舰载机降落的拦阻索是一种特种钢缆,属新型无机非金属材料 |
| A. | 加入少量的H2SO4溶液 | B. | 加入少量NaCl溶液 | ||
| C. | 加热 | D. | 加入少量NaOH溶液 |