题目内容
在2L密闭容器中,在一定条件下发生A(g)+3B(g) 2C(g),在10s内反应物A的浓度由1mol/L降到0.6mol/L,则ν(C)为( )
2C(g),在10s内反应物A的浓度由1mol/L降到0.6mol/L,则ν(C)为( )
 2C(g),在10s内反应物A的浓度由1mol/L降到0.6mol/L,则ν(C)为( )
2C(g),在10s内反应物A的浓度由1mol/L降到0.6mol/L,则ν(C)为( )分析:根据v=
计算v(A),再利用速率之比等于化学计量数之比计算v(C).
| △c |
| △t |
解答:解:在10s内反应物A的浓度由1mol/L降到0.6mol/L,所以v(A)=
=0.04mol/(L?s),
由反应速率之比等于化学计量数之比,所以v(C)=2v(A)=2×0.04mol/(L?s)=0.08mol/(L?s),
故选A.
| 1mol/L-0.6mol/L |
| 10s |
由反应速率之比等于化学计量数之比,所以v(C)=2v(A)=2×0.04mol/(L?s)=0.08mol/(L?s),
故选A.
点评:本题考查化学反应速率的计算,难度较小,旨在考查学生对基础知识的掌握.可以利用定义法,也可利用计量数法计算.

练习册系列答案
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案
相关题目
某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如表所示.
(1)根据下表中数据,在该题坐标图上画出X、Z的物质的量(n)随时间(t)变化的曲线:(图中已画出Y,用铅笔作图,并在你画出的曲线末端明确标出“x”或“z”)
(2)体系中发生反应的化学方程式是______;
(3)列式并计算该反应在0-5min时间内产物Z的平均反应速率:______;
(4)该反应在第______分钟(min)时达到平衡状态;
(5)若使该反应的速率增加,下列措施一定不能达到目的是______.
A.升高温度 B.降低温度
C.使用催化剂 D.保持容器体积不变加入1molx和2moly.
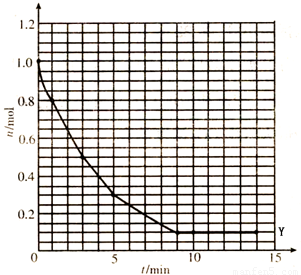
(1)根据下表中数据,在该题坐标图上画出X、Z的物质的量(n)随时间(t)变化的曲线:(图中已画出Y,用铅笔作图,并在你画出的曲线末端明确标出“x”或“z”)
| t/min | X/mol | Y/mool | Z/mol |
| 1.00 | 1.00 | 0.00 | |
| l | 0.90 | 0.80 | 0.20 |
| 3 | 0.75 | 0.50 | 0.50 |
| 5 | 0.65 | 0.30 | 0.70 |
| 9 | 0.55 | 0.10 | 0.90 |
| 10 | 0.55 | 0.10 | 0.90 |
| 14 | 0.55 | 0.10 | 0.90 |
(3)列式并计算该反应在0-5min时间内产物Z的平均反应速率:______;
(4)该反应在第______分钟(min)时达到平衡状态;
(5)若使该反应的速率增加,下列措施一定不能达到目的是______.
A.升高温度 B.降低温度
C.使用催化剂 D.保持容器体积不变加入1molx和2moly.

 (2)体系中发生反应的化学方程式是
(2)体系中发生反应的化学方程式是 2NH3(g) △H。下图I是合成氨反应的能量与反应过程相关图(未使用催化剂);图D是合成気反应在2L容器中、相同投料情况下、其它条件都不变时,某一反应条件的改变对反应的影响图。
2NH3(g) △H。下图I是合成氨反应的能量与反应过程相关图(未使用催化剂);图D是合成気反应在2L容器中、相同投料情况下、其它条件都不变时,某一反应条件的改变对反应的影响图。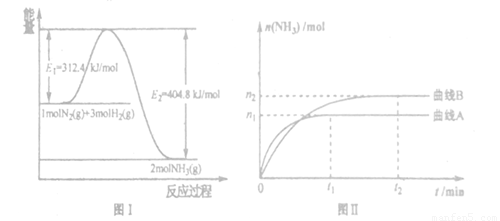
 mol/(L·min)
mol/(L·min) 倍,则此温度下的平衡常数为_______。在同一温度,同一容器中,将起始物质改为amol N2 b molH2 c mol NH3 (a,b,c均不为零)欲使平衡混合物中各物质的质量与原平衡相同,则a,b,c满足的关系为_____________(用含a,b,c的表达式表示),且欲使反应在起始时向逆反应方向进行,c的取值范围是_______
倍,则此温度下的平衡常数为_______。在同一温度,同一容器中,将起始物质改为amol N2 b molH2 c mol NH3 (a,b,c均不为零)欲使平衡混合物中各物质的质量与原平衡相同,则a,b,c满足的关系为_____________(用含a,b,c的表达式表示),且欲使反应在起始时向逆反应方向进行,c的取值范围是_______