题目内容
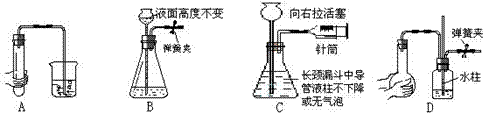
欲用亚硫酸钠和硫酸制取0.5mol的二氧化硫气体,要用下列仪器来组装气体发生装置,应选用的仪器是 ( )
| A.试管 | B.烧瓶 | C.烧杯 | D.集气瓶 |
B
中学阶段常见的容器和反应器有:试管、烧杯、烧瓶、锥形瓶、坩埚、蒸发皿、集气瓶、试剂瓶、滴瓶、启普发生器等。要求掌握这些仪器的主要用途和使用注意事项,如能否直接加热、所装试剂的量等。本题所给仪器都可做反应容器,但烧杯、集气瓶一般不用来装配气体发生装置,试管和烧瓶都可以做反应容器,但试管适用于少量物质间的反应,而烧瓶可适用于较多量物质间的反应,现欲配制0.5mol二氧化硫气体,至少需亚硫酸钠固体63g,故应选烧瓶。

练习册系列答案
 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目


 我国中医药已逐步进入国际市场,但国外在进口中药时对中草药中的重金属元素和有毒元素的含量等各项指标检查是非常严格的。下面是某分析实验室对中草药中可能的残余有毒元素As的检验方法和步骤(As在中草药中主要以As2O3的形式存在):
我国中医药已逐步进入国际市场,但国外在进口中药时对中草药中的重金属元素和有毒元素的含量等各项指标检查是非常严格的。下面是某分析实验室对中草药中可能的残余有毒元素As的检验方法和步骤(As在中草药中主要以As2O3的形式存在): 从铝土矿(主要成分是
从铝土矿(主要成分是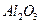 ,含
,含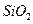 、
、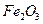 、MgO等杂质)中提取两种工艺品的流程如下:
、MgO等杂质)中提取两种工艺品的流程如下: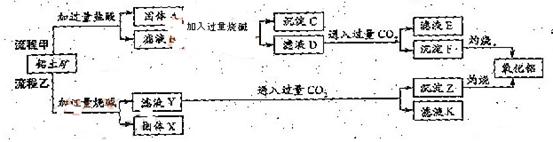
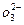 的离子方程式为________.
的离子方程式为________.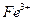 ,可取少量滤液并加入________(填试剂名称)。
,可取少量滤液并加入________(填试剂名称)。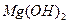 的容度积常数
的容度积常数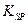 =5.6×
=5.6×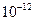 ,取适量的滤液B,加入一定量的烧碱达到沉淀溶液平衡,测得PH=13.00,则此温度下残留在溶液中的
,取适量的滤液B,加入一定量的烧碱达到沉淀溶液平衡,测得PH=13.00,则此温度下残留在溶液中的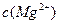 =_______.
=_______.