题目内容
【题目】以铁片和铜片为两极,以稀硫酸为电解质溶液组成原电池,当导线中通过2mol电子时,下列说法正确的是( )
A. 铁片溶解1 mol,铜片上析出1 mol H2
B. 两极上溶解和析出的物质的质量相等
C. 铁片溶解2 g,铜片上析出1 g H2
D. 铁片溶解1 mol,转移电子1 mol
【答案】A
【解析】
铁的金属性强于铜,铁是负极,从电极反应式看:负极:Fe-2e-=Fe2+;正极:2H++2e-=H2↑。当溶解1 mol铁即56g铁时失去2 mol电子,铜片上析出1 mol氢气即2g氢气得到2 mol电子,得失电子守恒,答案选A。

 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案【题目】某学习小组设计以下三个实验探究氯水的组成,请根据下表回答问题。
实验序号 | 实验方法 | 实验现象 | 结论 |
① | 将氯水滴加到AgNO3溶液中 | a: | 氯水中含有Cl- |
② | 将氯水滴加到含酚酞的NaOH溶液中 | 红色溶液 变为无色 | …… |
③ | 将氯水滴加到Na2CO3溶液中 | b: | 氯水中含有H+ |
(1)写出实验①和③的实验现象。
a:________________,b:________________。
(2)有同学认为实验③产生的现象是因为氯水中含有次氯酸,你是否同意这个观点?________(填“同意”或“不同意”),理由是________________________________________________。
(3)在分析实验②中实验现象产生的原因时,同学们的意见出现了分歧。甲同学认为氯水加到NaOH溶液中发生了中和反应而使溶液退色,乙同学认为氯水中含有的次氯酸具有漂白性而使溶液褪色。请你设计简单的实验证明他们的观点:______________________________________________。
【题目】高铁酸钾(K2FeO4)是一新型、高效、无毒的多功能水处理剂。
(资料)K2FeO4为紫色固体,微溶于KOH溶液,具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
(1)制备K2FeO4。
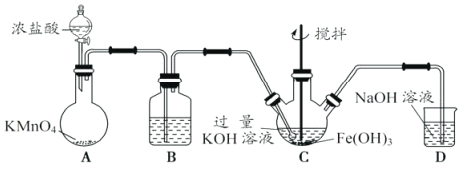
①A为制取氯气发生装置,其中盛放浓盐酸的仪器名称为___________。
②除杂装置B中的试剂为___________。
③C为制备K2FeO4装置,KOH溶液过量的原因是___________。
④D为尾气处理装置,发生反应的离子方程式为___________。
(2)探究 K2FeO4的性质。取C中紫色溶液,加入稀硫酸,产生黃绿色气体,得溶液a,经检验气体中含有Cl2。为证明K2FeO4能否氧化Cl-而产生Cl2,设计以下方案:
方案I | 取少量溶液a,滴加KSCN溶液至过量,溶液呈红色。 |
方案Ⅱ | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b。取少量b,滴加盐酸,有Cl2产生。 |
①由方案I中溶液变红可知a中含有___________。该离子的产生___________(填“能”或“不能”)判断一定是由K2FeO4被Cl-还原而形成的。
②方案Ⅱ用KOH溶液洗涤的目的是___________。方案Ⅱ得出氧化性:Cl2___________FeO42-(填“>”或“<”)
(3)使用时经常通过测定高铁酸钾的纯度来判断其是否变质。K2FeO4在硫酸溶液中反应如下:_______ FeO42-+______H+===_______O2↑+________Fe3++________(配平及完成上述离子方程式)________。现取C中洗涤并干燥后样品的质量10g,加入稀硫酸,收集到0.672L气体(标准状况下)。则样品中高铁酸钾的质量分数约为___________。(计算结果保留到0.1%)