题目内容
【题目】设NA表示阿伏伽德罗常数的值,下列说法正确的是( )
A.1 g H2含有的分子数为0.5NA
B.标准状况下,2.24 L H2O含有的分子数为0.1NA
C.1 L 0.1mol/L MgCl2溶液中含有的Cl-数为0.1NA
D.1 mol NaOH固体含有的离子总数为3NA
【答案】A
【解析】
A.1gH2的物质的量为![]() =0.5mol,所含分子数为0.5NA,故A正确;
=0.5mol,所含分子数为0.5NA,故A正确;
B.标况下H2O不是气体状态,不能用气体摩尔体积计算其物质的量,因此无法计算所含分子具体数目,故B错误;
C.1L0.1mol/LMgCl2溶液中n(MgCl2)=1L×0.1mol/L=0.1mol,所含Cl-数为0.2NA,故C错误;
D.NaOH中所含离子为Na+、OH-,因此1molNaOH固体含有的离子总数为2NA,故D错误;
故答案为:A。

练习册系列答案
相关题目
【题目】2019年是元素周期表诞生150周年,元素周期表在学习、研究和生产实践中有很重要的作用。①~⑥六种元素在元素周期表中的位置如下:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
1 | ① | ||||||
2 | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ |
请回答下列问题:
(1)⑥的元素符号为___________。
(2)由①③④形成的化合物是一种强碱,其化学式____________。
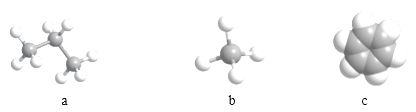
(3)由①②形成的最简单化合物的分子模型为_____________(填序号)
(4)⑤和⑥两种元素的最高价氧化物对应的水化物之间反应的离子方程式为________________________________。