题目内容
I.氢能的存储是氢能应用的主要瓶颈,配位氢化物、富氢载体化合韧是目前所采用的主要储氢材料。
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。在基态Ti2+中,电子占据的最高能层符号为 ,该能层具有的原子轨道数为 ;
(2)液氨是富氢物质,是氢能的理想载体,利用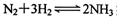 实现储氢和输氢。下列说法正确的是 ;
实现储氢和输氢。下列说法正确的是 ;
a.NH3分子中氮原子的轨道杂化方式为sp2杂化
b.NH+4与PH+4、CH4、BH-4、ClO—4互为等电子体
c.相同压强时,NH3的沸点比PH3的沸点高
d.[Cu(NH3)4]2+离子中,N原子是配位原子
(3)已知NF3与NH3的空间构型相同,但NF3不易与Cu2+形成配离子,其原因是 ;
II.氯化钠是生活中的常用调味品,也是结构化学中研究离子晶体时常用的代表物,其晶胞结构如图所示。
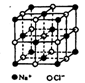
(1)设氯化钠晶体中Na+与跟它最近邻的Cl—之间的距离为r,则该Na+与跟它次近邻的C1—个数为 ,该Na+与跟它次近邻的Cl—之间的距离为 ;
(2)已知在氯化钠晶体中Na+的半径为以a pm,Cl—的半径为b pm,它们在晶
体中是紧密接触的,则在氯化钠晶体中离子的空间利用率为 ;(用含a、b的式子袁示)
(3)纳米材料的表面原子占总原子数的比例很大,这是它有许多特殊性质的原因。假设某氯化钠颗粒形状为立方体,边长为氯化钠晶胞的10倍,则该氯化钠颗粒中表面原子占总原子数的百分比为 。
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。在基态Ti2+中,电子占据的最高能层符号为 ,该能层具有的原子轨道数为 ;
(2)液氨是富氢物质,是氢能的理想载体,利用
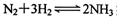 实现储氢和输氢。下列说法正确的是 ;
实现储氢和输氢。下列说法正确的是 ;a.NH3分子中氮原子的轨道杂化方式为sp2杂化
b.NH+4与PH+4、CH4、BH-4、ClO—4互为等电子体
c.相同压强时,NH3的沸点比PH3的沸点高
d.[Cu(NH3)4]2+离子中,N原子是配位原子
(3)已知NF3与NH3的空间构型相同,但NF3不易与Cu2+形成配离子,其原因是 ;
II.氯化钠是生活中的常用调味品,也是结构化学中研究离子晶体时常用的代表物,其晶胞结构如图所示。

(1)设氯化钠晶体中Na+与跟它最近邻的Cl—之间的距离为r,则该Na+与跟它次近邻的C1—个数为 ,该Na+与跟它次近邻的Cl—之间的距离为 ;
(2)已知在氯化钠晶体中Na+的半径为以a pm,Cl—的半径为b pm,它们在晶
体中是紧密接触的,则在氯化钠晶体中离子的空间利用率为 ;(用含a、b的式子袁示)
(3)纳米材料的表面原子占总原子数的比例很大,这是它有许多特殊性质的原因。假设某氯化钠颗粒形状为立方体,边长为氯化钠晶胞的10倍,则该氯化钠颗粒中表面原子占总原子数的百分比为 。
Ⅰ.(1)M(1分) 9(2分)
(2)cd(2分)
(3)N、F、H三种元素的电负性为F > N >H,在NF3中,共用电子对偏向F,偏离N原子,使得氮原子上的孤电子对难于与Cu2+形成配位键(2分)
Ⅱ.(1)8(2分)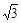 r(2分)
r(2分)
(2)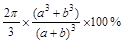 (2分)
(2分)
(3)26% 或 (2分)
(2分)
(2)cd(2分)
(3)N、F、H三种元素的电负性为F > N >H,在NF3中,共用电子对偏向F,偏离N原子,使得氮原子上的孤电子对难于与Cu2+形成配位键(2分)
Ⅱ.(1)8(2分)
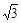 r(2分)
r(2分) (2)
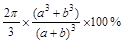 (2分)
(2分) (3)26% 或
 (2分)
(2分)试题分析:Ⅰ.(1)Ti原子核外有22个电子,其基态原子的核外电子排布式为1s22s22p63s23p63d24s2,在基态Ti2+中,核外电子排布式为1s22s22p63s23p63d2,对应能层分别别为K、L、M,其中能量最高的是最外层M层,该能层有s、p、d三个能级,s能级有1个轨道,p能级有3个轨道,d能级有5个轨道,所以共有9个原子轨道。
(2)a.NH3分子中N原子含有3个共用电子对和一个孤电子对,所以其价层电子对是4,采用sp3杂化,故错误。
b.等电子体是指具有相同电子数目和原子数目的分子或离子,NH4+与PH4+、CH4、BH4-、ClO4—原子数目相同,电子数目不同,所以不能互为等电子体,故错误。
c.相同压强时,氨气中含有氢键,PH3中不含氢键,所以NH3沸点比PH3高,故正确;
d..[Cu(NH3)4]2+离子中,N原子提供孤电子对,所以N原子是配位原子,故正确。
所以选cd 。
(3)N、F、H三种元素的电负性:F>N>H,所以NH3中共用电子对偏向N,而在NF3中,共用电子对偏向F,偏离N原子,故答案为:F的电负性比N大,N-F成键电子对向F偏移,导致NF3中N原子核对其孤对电子的吸引能力增强,难以形成配位键,故NF3不易与Cu2+形成配离子(或者N、F、H三种元素的电负性:F>N>H,在NF3中,共用电子对偏向F,偏离N原子使得氮原子上的孤对电子难于与Cu2+形成配位键.);
Ⅱ.(1)氯化钠晶体中,
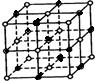 ,从图中可以看出,钠离子在体心和棱心位置,氯离子在顶点和面心位置,Na+与跟它次近邻的C1—(也就是图中晶胞大立方体中的8个顶点小白圈 )个数为8个,该Na+与跟它次近邻的Cl—之间的距离也就是边长为r的小立方体的体对角线,也就是
,从图中可以看出,钠离子在体心和棱心位置,氯离子在顶点和面心位置,Na+与跟它次近邻的C1—(也就是图中晶胞大立方体中的8个顶点小白圈 )个数为8个,该Na+与跟它次近邻的Cl—之间的距离也就是边长为r的小立方体的体对角线,也就是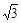 r 。
r 。(2)晶胞为面心立方,一个氯化钠晶胞中有4个Na+和Cl-,这个正方体的边长是2(a+b)pm,体积是8(a+b)3pm3,一个Na+体积是
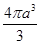 pm3,一个Cl-体积是
pm3,一个Cl-体积是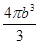 pm3,4个Na+和Cl-体积是
pm3,4个Na+和Cl-体积是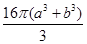 pm3,氯化钠晶体中离子的空间利用率为
pm3,氯化钠晶体中离子的空间利用率为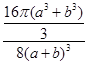 ×100%=
×100%=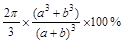 。
。(3)由NaCl的晶胞图可知,NaCl的晶胞为正立方体结构,立方体的体心只有一个Na+,而其它的离子都处在立方体的面上,边长为氯化钠晶胞边长的10倍的氯化钠颗粒中总原子数为21的立方,而其内部的总原子数为19的立方(立方体相对的两个面上各被剥去了一层原子,所以整个边长相当于是减少了2,所以是19),所以该氯化钠颗粒中表面原子占总原子数的百分比为
 =26%,另外列一种比较直观明了的解法: 由于立方体中的总原子数为n3(n为棱上原子数) 因此边长为氯化钠晶胞边长的10倍的氯化钠颗粒中总原子数为213,而其内部的总原子数为193(相当于将外面剥掉一层),所以其表面的原子数为213-193。表面原子占总原子数的百分数:
=26%,另外列一种比较直观明了的解法: 由于立方体中的总原子数为n3(n为棱上原子数) 因此边长为氯化钠晶胞边长的10倍的氯化钠颗粒中总原子数为213,而其内部的总原子数为193(相当于将外面剥掉一层),所以其表面的原子数为213-193。表面原子占总原子数的百分数: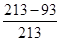 =26%。
=26%。
练习册系列答案
 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案
相关题目
 CH2、②HC≡CH、③
CH2、②HC≡CH、③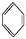 、④HCHO,其中碳原子采取sp2杂化的分子有 (填物质序号),HCHO分子的立体结构为 形。
、④HCHO,其中碳原子采取sp2杂化的分子有 (填物质序号),HCHO分子的立体结构为 形。 




 键与
键与 键的个数比为 。
键的个数比为 。