题目内容
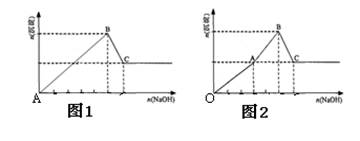
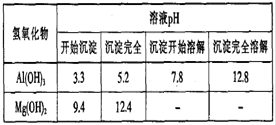
(3分)取两等份铝粉,第一份加入250 mL 2 mol·L-1的盐酸,第二份加入400 mL2mol·L-1的烧碱。若同温同压下放出气体体积之比为5:6,则加入的铝粉每份质量为 。
5.4g
由方程式可知:①2Al+6H+=2Al3++3H2↑ ②2Al+2OH-+2H2O=2AlO2-+3H2↑
当铝均不足时,所产生气体的体积比为1:1,当铝均过量时,所产生气体的体积比为1:3,而本题所得气体之比为1:1.2,故铝与酸反应时,酸不足,而与碱反应时,铝不足
故由①可知,250 mL 2 mol·L-1的盐酸生成的气体为0.25×2/2=0.25mol,进而可计算出由②产生的氢气为0.25×6/5=0.3mol,对应的铝粉的质量为:0.2×27=5.4g
当铝均不足时,所产生气体的体积比为1:1,当铝均过量时,所产生气体的体积比为1:3,而本题所得气体之比为1:1.2,故铝与酸反应时,酸不足,而与碱反应时,铝不足
故由①可知,250 mL 2 mol·L-1的盐酸生成的气体为0.25×2/2=0.25mol,进而可计算出由②产生的氢气为0.25×6/5=0.3mol,对应的铝粉的质量为:0.2×27=5.4g

练习册系列答案
相关题目
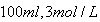 的盐酸和
的盐酸和 溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得生成的气体体积比为甲:乙=1:2,则加入铝粉的质量为( )
溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得生成的气体体积比为甲:乙=1:2,则加入铝粉的质量为( )