题目内容
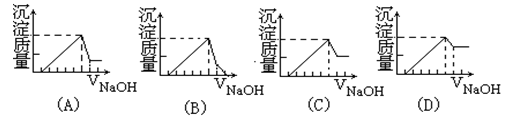
有一块镁铝合金,其中镁与铝的质量比是8:9。加入足量稀H2SO4使其完全溶解后,再加入NaOH溶液,生成沉淀的质量随NaOH溶液体积变化的曲线如下图,其中正确的是( )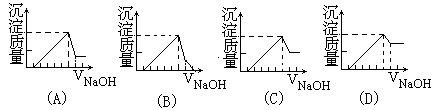

A
镁铝溶解:Mg+2H+=Mg2++H2↑ 2Al+6H+=2Al3++3H2↑
向溶解后的溶液中再加入NaOH溶液:H++OH-=H2O Mg2++2OH-=Mg(OH)2↓ Al+3OH-=Al(OH)3↓ Al(OH)3+OH-=AlO2-+2H2O
原合金中镁铝两金属的物质的量比为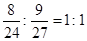 ,可设两者均为1mol,则
,可设两者均为1mol,则
离子沉淀完全所消耗的OH-为5mol,生成Mg(OH)2、Al(OH)3沉淀各1mol,质量共58+78=136g,Al(OH)3溶解后,沉淀只剩下Mg(OH)2,其质量为58g,对比各图像可知,A符合答案
向溶解后的溶液中再加入NaOH溶液:H++OH-=H2O Mg2++2OH-=Mg(OH)2↓ Al+3OH-=Al(OH)3↓ Al(OH)3+OH-=AlO2-+2H2O
原合金中镁铝两金属的物质的量比为
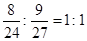 ,可设两者均为1mol,则
,可设两者均为1mol,则离子沉淀完全所消耗的OH-为5mol,生成Mg(OH)2、Al(OH)3沉淀各1mol,质量共58+78=136g,Al(OH)3溶解后,沉淀只剩下Mg(OH)2,其质量为58g,对比各图像可知,A符合答案

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案
相关题目
 Y溶液中分别加入NaOH和HCl时产生沉淀的物质的量与加入盐酸和氢氧化钠溶液体积之间的关系,下列说法正确的是( )
Y溶液中分别加入NaOH和HCl时产生沉淀的物质的量与加入盐酸和氢氧化钠溶液体积之间的关系,下列说法正确的是( )
 中,比较两种操作是
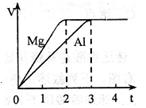
中,比较两种操作是 气体的体积(V)与时间(t)关系如图。反应中镁和铝的
气体的体积(V)与时间(t)关系如图。反应中镁和铝的