��Ŀ����
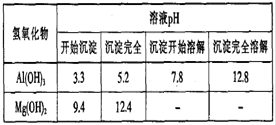
Mg2+��Al3+�Ļ����Һ����μ���NaOH��Һ���γɳ����������������ͼʾ��ͼ1Ϊ��ͬѧ���ƣ�ͼ2����ͬѧ����ʵ�������ƣ����ij������ɺ�Al(OH)3�ܽ��pH������������˵����ȷ���ǣ� ��
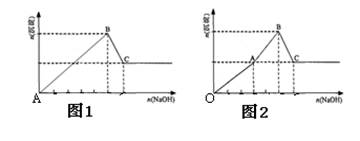


| A����ͼ�����n(Mg2+): n(Al3+)=2:1 |
| B��ͼ1ʵ���У�OA���������ֳ��� |
| C������������Ϣ�ó���Ӧ���¶��£�Ksp(Al(OH)3)> Ksp(Mg(OH)2) |
| D����ϱ������ݺ�ͼ2������AB�ο��ܷ�����Mg2++2AlO2��+4H2O ��2Al(OH)3��+Mg(OH)2�� |
D
A ����ͼ�����n(Mg2+): n(Al3+)=1:1
B ����ͼ1ʵ���У�û�б�OA��
C ����������Ϣֻ�Ǹ��Ŀ�ʼ������PH��û�и�������Ũ�ȵĴ�С�����ԣ��ò�������Ksp�Ĵ�С
D ��ȷ��þ���Ӻ�ƫ��������ӷ���˫ˮ�⡣
B ����ͼ1ʵ���У�û�б�OA��
C ����������Ϣֻ�Ǹ��Ŀ�ʼ������PH��û�и�������Ũ�ȵĴ�С�����ԣ��ò�������Ksp�Ĵ�С
D ��ȷ��þ���Ӻ�ƫ��������ӷ���˫ˮ�⡣

��ϰ��ϵ�д�
�����Ŀ
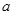 g��Ʒ�������м���������NaOH��Һ��������ɵ����壨��״������ͬ�����Ϊ
g��Ʒ�������м���������NaOH��Һ��������ɵ����壨��״������ͬ�����Ϊ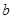 L����Ӧ�Ļ�ѧ����ʽ��_________________����Ʒ������������____________g��
L����Ӧ�Ļ�ѧ����ʽ��_________________����Ʒ������������____________g�� L���������루1������������������
L���������루1������������������ ��_________��
��_________��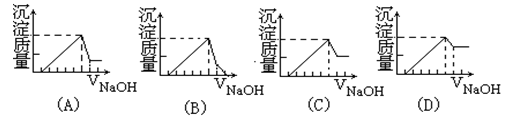
 Y��Һ�зֱ����NaOH��HClʱ�������������ʵ�����������������������Һ���֮��Ĺ�ϵ������˵����ȷ����(����)
Y��Һ�зֱ����NaOH��HClʱ�������������ʵ�����������������������Һ���֮��Ĺ�ϵ������˵����ȷ����(����)