题目内容
实验室需要配制1.0mol/L硫酸溶液500mL,根据溶液配制情况回答下列问题:
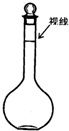
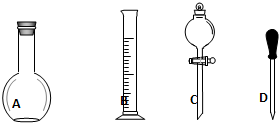
(1)实验中除了烧杯、量筒、玻璃棒外还需要的其它仪器有:______.
(2)根据计算得知,所需质量分数为98%、密度为1.84g/cm3的浓硫酸体积为______mL.(计算结果保留一位小数)
(3)配制一定物质的量浓度溶液的实验中,如果出现以下操作:
A.量取浓硫酸的量筒内有少量水;
B.浓硫酸在烧杯中溶解后,未经冷却就立即转移到容量瓶中;
C.住容量瓶转移时,有少量液体溅出
D.将量筒洗涤后洗涤液一并转入容量瓶
E.定容时仰视刻度线
F.容量瓶未干燥即用来配制溶液
G.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线.
对配制的溶液物质的量浓度可能造成偏大的有______(填写字母);无影响有______.
(1)实验中除了烧杯、量筒、玻璃棒外还需要的其它仪器有:______.
(2)根据计算得知,所需质量分数为98%、密度为1.84g/cm3的浓硫酸体积为______mL.(计算结果保留一位小数)
(3)配制一定物质的量浓度溶液的实验中,如果出现以下操作:
A.量取浓硫酸的量筒内有少量水;
B.浓硫酸在烧杯中溶解后,未经冷却就立即转移到容量瓶中;
C.住容量瓶转移时,有少量液体溅出
D.将量筒洗涤后洗涤液一并转入容量瓶
E.定容时仰视刻度线
F.容量瓶未干燥即用来配制溶液
G.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线.
对配制的溶液物质的量浓度可能造成偏大的有______(填写字母);无影响有______.
(1)配制500ml1.0mol/L稀硫酸,操作步骤有计算、量取、稀释、移液、洗涤移液、定容、摇匀等操作,用筒量取(用到胶头滴管)浓硫酸,在烧杯中稀释,用玻璃棒搅拌,冷却后转移到500mL容量瓶中,并用玻璃棒引流,洗涤2-3次,将洗涤液转移到容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀.
所以需要的仪器为:烧杯、筒量、玻璃棒、500mL容量瓶、胶头滴管.
所以还需要的仪器是:500mL容量瓶、胶头滴管,故答案为:500mL容量瓶、胶头滴管;
(2)质量分数为98%、密度为1.84g/cm3的浓硫酸的物质的量浓度为
mol/L=18.4mol/L,根据稀释定律,稀释前后溶质的物质的量不变,设浓硫酸的体积为xmL,所以xmL×18.4mol/L=500mL×1.0mol/L,解得:x≈27.2,故答案为:27.2;
(3)A.量取浓硫酸的量筒内有少量水,量取浓硫酸的体积偏小,所配溶液浓度偏小;
B.浓硫酸在烧杯中溶解后,未经冷却就立即转移到容量瓶中进行定容,溶液冷却后导致所配溶液的体积偏小,溶液浓度偏大;
C.住容量瓶转移时,有少量液体溅出,移入容量瓶内的硫酸减少,所配溶液浓度偏小;
D.量筒为流量式仪器,将量筒洗涤后洗涤液一并转入容量瓶,移入容量瓶内硫酸增大,所配溶液浓度偏大;
E.定容时仰视刻度线,导致所配溶液的体积偏大,溶液浓度偏小;
F.溶液配制需加水定容,容量瓶未干燥即用来配制溶液,对所配溶液浓度无影响;
G.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,少量溶液残留在瓶塞与瓶口之间,再加水至刻度线,所配溶液的体积偏大,溶液浓度偏小.
对配制的溶液物质的量浓度可能造成偏大的有BD;无影响有F.
故答案为:BD;F.
所以需要的仪器为:烧杯、筒量、玻璃棒、500mL容量瓶、胶头滴管.
所以还需要的仪器是:500mL容量瓶、胶头滴管,故答案为:500mL容量瓶、胶头滴管;
(2)质量分数为98%、密度为1.84g/cm3的浓硫酸的物质的量浓度为
| 1000×1.84×98% |
| 98 |
(3)A.量取浓硫酸的量筒内有少量水,量取浓硫酸的体积偏小,所配溶液浓度偏小;
B.浓硫酸在烧杯中溶解后,未经冷却就立即转移到容量瓶中进行定容,溶液冷却后导致所配溶液的体积偏小,溶液浓度偏大;
C.住容量瓶转移时,有少量液体溅出,移入容量瓶内的硫酸减少,所配溶液浓度偏小;
D.量筒为流量式仪器,将量筒洗涤后洗涤液一并转入容量瓶,移入容量瓶内硫酸增大,所配溶液浓度偏大;
E.定容时仰视刻度线,导致所配溶液的体积偏大,溶液浓度偏小;
F.溶液配制需加水定容,容量瓶未干燥即用来配制溶液,对所配溶液浓度无影响;
G.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,少量溶液残留在瓶塞与瓶口之间,再加水至刻度线,所配溶液的体积偏大,溶液浓度偏小.
对配制的溶液物质的量浓度可能造成偏大的有BD;无影响有F.
故答案为:BD;F.

练习册系列答案
相关题目