题目内容
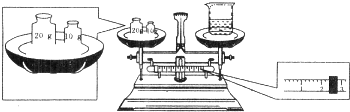
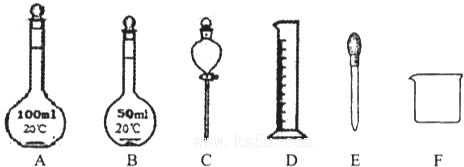
(1)用已准确称量的1.06gNa2CO3固体配制0.100mol/LNa2CO3溶液100mL,所需要的仪器为:______.
(2)为除去粗盐中的CaCl2、MgCl2、Na2SO4杂质,依次加入的溶液为(填物质的化学式):______、______、______、______.
(2)为除去粗盐中的CaCl2、MgCl2、Na2SO4杂质,依次加入的溶液为(填物质的化学式):______、______、______、______.
(1)配制步骤有计算、称量、溶解、冷却、移液、洗涤、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解,冷却后转移到100mL容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,所以需要的仪器为:托盘天平、药匙、烧杯、玻璃棒、100mL容量瓶、胶头滴管,
故答案为:烧杯、玻璃棒、100mL容量瓶、胶头滴管;
(2)首先要把粗盐溶于水形成溶液,然后镁离子用氢氧根离子沉淀,加入过量的氢氧化钠可以将镁离子沉淀,硫酸根离子用钡离子沉淀,加入过量的氯化钡可以将硫酸根离子沉淀,至于先除镁离子,还是先除硫酸根离子都行,钙离子用碳酸根离子沉淀,除钙离子加入碳酸钠转化为沉淀,Ca2++CO32-=CaCO3↓,但是加入的碳酸钠要放在加入的氯化钡之后,这样碳酸钠会除去反应剩余的氯化钡,Ba2++CO32-=BaCO3↓,离子都沉淀了,再进行过滤,为使离子沉淀完全,最后加入盐酸将氢氧化钠和碳酸钠除掉,需要加入的试剂都必须是过量;
故答案为:BaCl2;NaOH;Na2CO3;HCl;
故答案为:烧杯、玻璃棒、100mL容量瓶、胶头滴管;
(2)首先要把粗盐溶于水形成溶液,然后镁离子用氢氧根离子沉淀,加入过量的氢氧化钠可以将镁离子沉淀,硫酸根离子用钡离子沉淀,加入过量的氯化钡可以将硫酸根离子沉淀,至于先除镁离子,还是先除硫酸根离子都行,钙离子用碳酸根离子沉淀,除钙离子加入碳酸钠转化为沉淀,Ca2++CO32-=CaCO3↓,但是加入的碳酸钠要放在加入的氯化钡之后,这样碳酸钠会除去反应剩余的氯化钡,Ba2++CO32-=BaCO3↓,离子都沉淀了,再进行过滤,为使离子沉淀完全,最后加入盐酸将氢氧化钠和碳酸钠除掉,需要加入的试剂都必须是过量;
故答案为:BaCl2;NaOH;Na2CO3;HCl;

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目