题目内容
10.酚是一类重要的化工原料,以苯酚为原料可实现阿司匹林等物质的合成.
已知:

(1)化合物A的分子式为C7H6O3,其分子中含氧官能团的名称是羧基、羟基.
(2)G的结构简式为
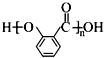 ;⑤的反应条件是NaOH的醇溶液、加热;⑧的反应类型是加聚反应.
;⑤的反应条件是NaOH的醇溶液、加热;⑧的反应类型是加聚反应.(3)阿司匹林与NaOH溶液完全反应的化学方程式为
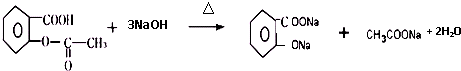 .
.(4)写出符合下列条件的B的任意一种同分异构体的结构简式
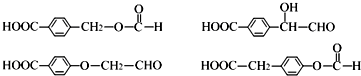 .
.a苯环上只有两个取代基;
b能发生银镜反应;
c能与NaHCO3溶液反应产生使澄清石灰水变浑浊的气体;
d分子中苯环上只有2种不同化学环境的氢.
(5)研究人员高效地实现了吲哚化合物与醇类、酚类、CO和O2在一定条件下直接发生插羰氢酯基化反应,结合反应①,试写出由2-甲基吲哚 (
 )合成2-甲基-3-甲酸甲酯吲哚的反应方程式
)合成2-甲基-3-甲酸甲酯吲哚的反应方程式 .
.
分析 苯酚发生取代反应生成邻羟基苯甲酸钠,邻羟基苯甲酸钠酸化得到水杨酸,A结构简式为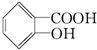 ,根据题给信息知,A发生取代反应、然后酸化生成B,B为阿司匹林,B构简式为
,根据题给信息知,A发生取代反应、然后酸化生成B,B为阿司匹林,B构简式为 ,A发生缩聚反应生成G,G结构简式为
,A发生缩聚反应生成G,G结构简式为 ;
;
苯酚和足量氢气发生加成反应生成D,D结构简式为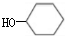 ,
, 发生消去反应生成E,E为
发生消去反应生成E,E为 ,E与溴发生加成反应生成
,E与溴发生加成反应生成 ,在氧化钠醇溶液、加热条件下发生消去反应生成F,则F为
,在氧化钠醇溶液、加热条件下发生消去反应生成F,则F为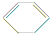 ,F发生加聚反应生成高聚物
,F发生加聚反应生成高聚物 ,据此分析解答.
,据此分析解答.
解答 解:苯酚发生取代反应生成邻羟基苯甲酸钠,邻羟基苯甲酸钠酸化得到水杨酸,A结构简式为 ,根据题给信息知,A发生取代反应、然后酸化生成B,B为阿司匹林,B构简式为
,根据题给信息知,A发生取代反应、然后酸化生成B,B为阿司匹林,B构简式为 ,A发生缩聚反应生成G,G结构简式为
,A发生缩聚反应生成G,G结构简式为 ;
;
苯酚和足量氢气发生加成反应生成D,D结构简式为 ,
, 发生消去反应生成E,E为
发生消去反应生成E,E为 ,E与溴发生加成反应生成
,E与溴发生加成反应生成 ,在氧化钠醇溶液、加热条件下发生消去反应生成F,则F为
,在氧化钠醇溶液、加热条件下发生消去反应生成F,则F为 ,F发生加聚反应生成高聚物
,F发生加聚反应生成高聚物 ,
,
(1)A结构简式为 ,其分子式为C7H6O3,该分子中含氧官能团是羧基、羟基,
,其分子式为C7H6O3,该分子中含氧官能团是羧基、羟基,
故答案为:C7H6O3;羟基、羧基;
(2)G为 ,⑤的反应是在氢氧化钠的醇溶液中加热发生消去反应;
,⑤的反应是在氢氧化钠的醇溶液中加热发生消去反应;
⑧的反应类型是加聚反应,
故答案为: ;NaOH的醇溶液、加热;加聚反应;
;NaOH的醇溶液、加热;加聚反应;
(3)阿司匹林与NaOH溶液完全反应的化学方程式为 ,
,
故答案为: ;
;
(4)B为 ,B的同分异构体符合下列条件:
,B的同分异构体符合下列条件:
a苯环上只有两个取代基;
b能发生银镜反应,说明含有醛基;
c能与NaHCO3溶液反应产生使澄清石灰水变浑浊的气体,说明含有羧基;
d分子中苯环上只有2种不同化学环境的氢,说明苯环上只有两种氢原子,
符合条件的同分异构体有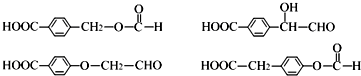 ,故答案为:
,故答案为: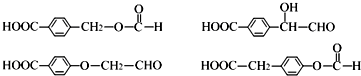 ;
;
(5)2-甲基吲哚 ( )合成2-甲基-3-甲酸甲酯吲哚的反应方程式为,故答案为:
)合成2-甲基-3-甲酸甲酯吲哚的反应方程式为,故答案为: ,
,
故答案为: .
.
点评 本题考查有机合成,侧重考查同分异构体的书写、反应条件判断、反应类型判断等知识点,根据流程图中反应条件、结构简式、分子式结合题给信息进行推断,注意正确分析题给信息并灵活运用,难点是(4)题同分异构体种类判断,题目难度中等.

| A. | 碳正离子[(CH3)3C+] | B. | PCl3 | C. | 尿素( ) ) | D. | HClO |
| A. | CH2═CHCl | B. |  | ||
| C. |  | D. | CH3-CH═CH2 |

| A. | 该烃X与等质量的甲烷相比,X燃烧时消耗的氧气更多 | |
| B. | 分子中碳原子的化学环境有2种 | |
| C. | 分子中的氢原子分布在两个互相垂直的直线上 | |
| D. | 分子中既有C-C键也有C=C键 |
 某研究性学习小组的同学通过对亚硫酸钠组成元素的价态进行分析后认为Na2SO3溶液在存放过程中有可能变质,若已变质,则相应反应的化学方程式2Na2SO3+O2=2Na2SO4.
某研究性学习小组的同学通过对亚硫酸钠组成元素的价态进行分析后认为Na2SO3溶液在存放过程中有可能变质,若已变质,则相应反应的化学方程式2Na2SO3+O2=2Na2SO4.

 (R、R′表示烃基或氢)
(R、R′表示烃基或氢) ,E的结构简式是CH3CHO.
,E的结构简式是CH3CHO.
 .
.