题目内容
6.芳香化合物A是一种基本化工原料,可以从煤和石油中得到.A、B、C、D、E的转化关系如图所示:
回答下列问题:
(1)A的化学名称是邻二甲苯(或1,2-二甲基苯);
(2)A→B 的反应类型是取代;
(3)A→C的化学方程式为
 ;
;(4)A与酸性KMnO4溶液反应可得到D,写出D的结构简式
 .
.
分析 A和溴发生取代反应生成B,根据B的结构简式知,A为邻二甲苯,其结构简式为 ,A和溴在催化剂条件下发生取代反应生成C,根据C的分子式知,C的结构简式为
,A和溴在催化剂条件下发生取代反应生成C,根据C的分子式知,C的结构简式为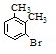 等,A被酸性高锰酸钾氧化生成D对二苯甲酸,其结构简式为
等,A被酸性高锰酸钾氧化生成D对二苯甲酸,其结构简式为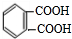 ,A与氢气发生加成反应生成E为
,A与氢气发生加成反应生成E为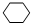 ,据此解答.
,据此解答.
解答 解:A和溴发生取代反应生成B,根据B的结构简式知,A为邻二甲苯,其结构简式为 ,A和溴在催化剂条件下发生取代反应生成C,根据C的分子式知,C的结构简式为
,A和溴在催化剂条件下发生取代反应生成C,根据C的分子式知,C的结构简式为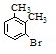 等,A被酸性高锰酸钾氧化生成D对二苯甲酸,其结构简式为
等,A被酸性高锰酸钾氧化生成D对二苯甲酸,其结构简式为 ,A与氢气发生加成反应生成E为
,A与氢气发生加成反应生成E为 ,
,
(1)A为 ,其名称是邻二甲苯(或1,2-二甲基苯),故答案为:邻二甲苯(或1,2-二甲基苯);
,其名称是邻二甲苯(或1,2-二甲基苯),故答案为:邻二甲苯(或1,2-二甲基苯);
(2)根据分子式变化知,A生成B的反应为取代反应,故答案为:取代;
(3)A为 ,C为
,C为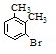 等,A和溴发生取代反应生成C,反应方程式为
等,A和溴发生取代反应生成C,反应方程式为 ,
,
故答案为: ;
;
(4)A为 ,A中甲基被酸性高锰酸钾溶液氧化生成羧基,所以D的结构简式为
,A中甲基被酸性高锰酸钾溶液氧化生成羧基,所以D的结构简式为 ,故答案为:
,故答案为: .
.
点评 本题考查有机物推断,侧重考查学生分析推断能力,为高频考点,以B结构简式为突破口结合反应条件进行推断,熟悉常见有机反应类型及反应条件,题目难度不大.

练习册系列答案
相关题目
16.按反应特征与产物的结构关系,有机反应大致可分为:取代反应、消去反应、加成反应三种,下列变化中不属于取代反应的是( )
| A. | C6H5CH2Cl+NaCN-→C6H5CH2CN+NaCl | B. | 2Na+2 C2H5OH-→2C2H5ONa+H2↑ | ||
| C. | CH3CH2CHO+HCN-→CH3CH2CH(CN)OH | D. | CH3COOC2H5+H2O-→CH3COOH+C2H5OH |
17.硫酸铅(PbSO4)广泛应用于制造铅蓄电池、白色颜料等.利用方铅矿精矿(PbS)直接制备硫酸铅粉末的流程如图1:
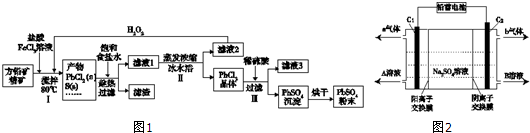
已知:(ⅰ)PbCl2(s)+2Cl-(aq)?PbCl42-(aq)△H>0
(ⅱ)有关物质的Ksp和沉淀时的pH如下:
(1)步骤Ⅰ中生成PbCl2的离子方程式PbS+2Fe3++2Cl-=PbCl2↓+2Fe2++S↓,加入盐酸控制pH值小于2,原因是抑制Fe3+、Pb2+的水解,防止生成Fe(OH)3、Pb(OH)2沉淀.
(2)用化学平衡移动原理解释步骤Ⅱ中使用冰水浴的原因用冰水浴使反应PbCl2(s)+2Cl-(aq)?PbCl42-(aq)逆向移动,使PbCl42-不断转化为PbCl2晶体而析出.若原料中FeCl3过量,则步骤Ⅱ得到的沉淀中还含有溶液中的悬浮杂质,溶液中的悬浮杂质被共同沉淀的原因是Fe3+水解生成Fe(OH)3胶体,吸附溶液中悬浮杂质,被共同沉淀.
(3)写出步骤Ⅲ中PbCl2晶体转化为PbSO4沉淀的离子方程式PbCl2(s)+SO42-(aq)=PbSO4(s)+2Cl-(aq).
(4)请用离子方程式解释滤液2加入H2O2可循环利用的原因2Fe2++H2O2+2H+=2Fe3++2H2O.
(5)铅蓄电池的电解液是硫酸,充电后两个电极上沉积的PbSO4分别转化为PbO2和Pb,充电时阴极的电极反应式为PbSO4+2e-=Pb+SO42-.
(6)双隔膜电解池的结构示意简图如图2所示,利用铅蓄电池电解硫酸钠溶液可以制取硫酸和氢氧化钠,并得到氢气和氧气.对该装置及其原理判断正确的是AD
A.A溶液为氢氧化钠,B溶液为硫酸
B.C1极与铅蓄电池的PbO2电极相接、C2极与铅蓄电池的Pb电极相接
C.当C1极产生标准状况下11.2L气体时,铅蓄电池的负极增重49g
D.该电解反应的总方程式可以表示为:2Na2SO4+6H2O$\frac{\underline{\;电解\;}}{\;}$2H2SO4+4NaOH+O2↑+2H2↑

已知:(ⅰ)PbCl2(s)+2Cl-(aq)?PbCl42-(aq)△H>0
| Ksp | 开始沉淀时pH | 完全沉淀时pH | ||
| PbSO4 | 1.08×10-8 | Fe (OH)3 | 2.7 | 3.7 |
| PbCl2 | 1.6×10-5 | Pb( OH)2 | 6 | 7.04 |
(1)步骤Ⅰ中生成PbCl2的离子方程式PbS+2Fe3++2Cl-=PbCl2↓+2Fe2++S↓,加入盐酸控制pH值小于2,原因是抑制Fe3+、Pb2+的水解,防止生成Fe(OH)3、Pb(OH)2沉淀.
(2)用化学平衡移动原理解释步骤Ⅱ中使用冰水浴的原因用冰水浴使反应PbCl2(s)+2Cl-(aq)?PbCl42-(aq)逆向移动,使PbCl42-不断转化为PbCl2晶体而析出.若原料中FeCl3过量,则步骤Ⅱ得到的沉淀中还含有溶液中的悬浮杂质,溶液中的悬浮杂质被共同沉淀的原因是Fe3+水解生成Fe(OH)3胶体,吸附溶液中悬浮杂质,被共同沉淀.
(3)写出步骤Ⅲ中PbCl2晶体转化为PbSO4沉淀的离子方程式PbCl2(s)+SO42-(aq)=PbSO4(s)+2Cl-(aq).
(4)请用离子方程式解释滤液2加入H2O2可循环利用的原因2Fe2++H2O2+2H+=2Fe3++2H2O.
(5)铅蓄电池的电解液是硫酸,充电后两个电极上沉积的PbSO4分别转化为PbO2和Pb,充电时阴极的电极反应式为PbSO4+2e-=Pb+SO42-.
(6)双隔膜电解池的结构示意简图如图2所示,利用铅蓄电池电解硫酸钠溶液可以制取硫酸和氢氧化钠,并得到氢气和氧气.对该装置及其原理判断正确的是AD
A.A溶液为氢氧化钠,B溶液为硫酸
B.C1极与铅蓄电池的PbO2电极相接、C2极与铅蓄电池的Pb电极相接
C.当C1极产生标准状况下11.2L气体时,铅蓄电池的负极增重49g
D.该电解反应的总方程式可以表示为:2Na2SO4+6H2O$\frac{\underline{\;电解\;}}{\;}$2H2SO4+4NaOH+O2↑+2H2↑
14.下列关于苯酚的叙述中,错误的是( )
| A. | 其水溶液显弱酸性,俗称石炭酸 | |
| B. | 其浓溶液对皮肤有强烈的腐蚀性,如果不慎沾在皮肤上,应立即用酒精擦洗 | |
| C. | 其在水中的溶解度随温度的升高而增大,超过65℃可以与水以任意比互溶 | |
| D. | 苯酚溶液不能使酸性高锰酸钾溶液褪色 |
1.下列反应的化学方程式或离子方程式表示正确的是( )
| A. | 1,3-丁二烯的1,2-加成:H2C=CHCH=CH2+Cl2→CH2ClCH=CHCH2Cl | |
| B. | 甲苯和氯气光照条件下发生反应: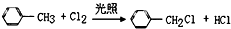 | |
| C. | 用醋酸去除水垢:CaCO3+2H+=Ca2++CO2↑+H2O | |
| D. | 用银氨溶液检验乙醛的醛基:CH3CHO+2Ag(NH4)2OH$\stackrel{水浴加热}{→}$CH3COONH4+3NH3+2Ag↓+H2O |
18.下列递变规律正确的是( )
| A. | N、O、F的原子半径依次增大 | B. | H2O、NH3、PH3的热稳定性依次增强 | ||
| C. | HCl、HBr、HI的还原性依次减弱 | D. | LiOH、KOH、CsOH的碱性依次增强 |
15.依据物质的相关数据,可以推断物质的结构和性质.下列推断不合理的是( )
| A. | 依据原子序数,推断该元素原子的核外电子数 | |
| B. | 依据相对分子质量,推断物质常温下的溶解度 | |
| C. | 依据气体的摩尔质量,推断相同状况下不同气体密度的大小 | |
| D. | 依据元素原子的最外层电子数,推测其可能的最高正价和最低化合价 |
16.下列叙述正确的是( )
| A. | H2 和D2 互为同位素 | |
| B. | 40Ca和40K中质子数和中子数都不相等 | |
| C. | 只含一种元素的物质一定是纯净物 | |
| D. | 18O中中子数和质子数相等 |