题目内容
【题目】20℃时,饱和KCl溶液的密度为1.174gcm﹣3 , 物质的量浓度为4.0molL﹣1 , 则下列说法中不正确的是( )
A.20℃时,饱和KCl溶液与等质量的水混合后物质的量浓度大于2.0molL﹣1
B.20℃时,将29.8 gKCl溶于87.6g水中可得饱和溶液
C.20℃时,密度小于1.174gcm﹣3的KCl溶液是不饱和溶液
D.将此溶液蒸发部分水,再恢复到20℃时,溶液中各离子的浓度不变
【答案】A
【解析】解:A、饱和KCl溶液与等质量的水混合后,水的密度小于氯化钾溶液,所以体积大于氯化钾溶液,所以混合后物质的量浓度小于2.0molL﹣1 , 故A错;
B、设饱和溶液的体积为1L,溶液的质量为1.174g/ml×1000ml=1174g,溶质的物质的量为1L×4.0mol/L=4mol,质量为4mol×74.5g/mol=298g,所以溶液的质量分数为 ![]() ×100%=25.38%,将29.8gKCl溶于
×100%=25.38%,将29.8gKCl溶于 ![]() ×100%=25.38%,两者相当,所以所得溶液为饱和溶液,故B正确;
×100%=25.38%,两者相当,所以所得溶液为饱和溶液,故B正确;
C、KCl溶液的浓度越大密度越大,故20℃时,密度小于1.174 gcm﹣3的KCl溶液是不饱和溶,故C正确;
D、若将饱和溶液蒸发,则有KCl晶体析出.再恢复到20℃时,其溶解度不变,溶液仍为饱和溶液,溶液中各离子的浓度不变,故D正确;
故选A.
【考点精析】关于本题考查的物质的量浓度的概念和溶解度、饱和溶液的概念,需要了解以单位体积里所含溶质B的物质的量来表示溶液组成的物理量,叫做溶质B的物质的量浓度;符号CB=nB(mol)/V(L) (nB是溶质B的物质的量,V是溶液体积),单位是mol·Lˉ1;在一定温度下,在一定量的溶剂里,不能再溶解某种溶质的溶液,叫作这种溶质的饱和溶液;还能继续溶解某种溶质的溶液,叫作不饱和溶液;在一定温度下,某固体物质在100克溶剂里达到饱和状态时所溶解的质量,叫作这种物质在这种物质在这种溶剂里的溶解度才能得出正确答案.

 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案【题目】利用如图装置测定中和热的实验步骤如下: ①量取50mL 0.25mol/L H2SO4溶液倒入小烧杯中,测量温度;
②量取50mL 0.55mol/L NaOH溶液,测量温度;
③将NaOH溶液倒入小烧杯中,混合均匀后测量混合液温度.请回答:
(1)如图所示,仪器A的名称是; 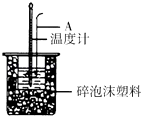
(2)NaOH溶液稍过量的原因 .
(3)加入NaOH溶液的正确操作是(填字母).
A.沿玻璃棒缓慢加入
B.一次迅速加入
C.分三次加入
(4)使硫酸与NaOH溶液混合均匀的正确操作是 .
(5)设溶液的密度均为1gcm﹣3 , 中和后溶液的比热容c=4.18J(g℃)﹣1 , 请根据实验数据写出该中和热的热化学方程式
温度 | 起始温度t1/℃ | 终止温度 | 温度差平均值 | ||
H2SO4 | NaOH | 平均值 | |||
1 | 25.0 | 25.2 | 28.5 | ||
2 | 24.9 | 25.1 | 28.3 | ||
3 | 25.5 | 26.5 | 31.8 | ||
4 | 25.6 | 25.4 | 29.0 | ||
(6)上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是(填字母) a.实验装置保温、隔热效果差
b.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
c.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
(7)怎样才能确保读取混合液的最高温度? .