题目内容
【题目】X、Y、Z为短周期元素,X的最外层电子数是Y原子最外层电子数的2倍,Y的原子序数比X的原子序数多5,Z原子的最外层电子数比Y多3。下列叙述正确的是( )
A.原子半径的大小顺序:Y>Z>X
B.Z单质与X单质直接反应可生成两种化合物
C.工业上,电解X和Y形成的化合物制取Y单质
D.Y、Z元素的最高价氧化物的水化物不能互相反应
【答案】AC
【解析】
根据描述,Y应该比X多一层电子,否则不可能在最外层电子数比X少的情况下,原子序数大于X。若X位于第一周期,Y不可能同时满足上面两条要求;若X位于第二周期,当X为氧,Y为铝时,可以同时满足上面两条要求,则Z为硫,据此来分析选项即可。
A.同周期主族元素,原子半径随原子序数的增大而减小,不同周期的元素,则周期越大半径越大,因此![]() ,A项正确;
,A项正确;
B.氧和硫直接反应只能得到![]() 一种化合物,B项错误;
一种化合物,B项错误;
C.工业上通过电解熔融氧化铝的方式来制取金属铝,C项正确;
D.Y、Z对应的最高价氧化物的水化物分别为![]() 和
和![]() ,二者可以反应,D项错误;
,二者可以反应,D项错误;
答案选AC。

 阅读快车系列答案
阅读快车系列答案【题目】等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产生氢气体积V的数据,根据数据绘制得到下图,则曲线a、b、c、d所对应的实验组别是
组别 | c(HCl)/molL-1 | 温度/℃ | 状态 |
1 | 2.0 | 25 | 块状 |
2 | 2.5 | 30 | 块状 |
3 | 2.5 | 50 | 粉末状 |
4 | 2.5 | 30 | 粉末状 |
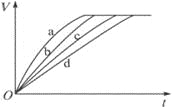
A.4-3-2-1
B.1-2-3-4
C.3-4-2-1
D.1-2-4-3
【题目】用惰性电极电解饱和食盐水(含少量Ca2+、Mg2+)并进行相关实验,电解一段时间后,各部分装置及对应的现象如下:
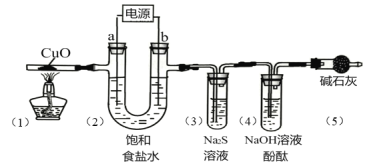
对应现象 | (1)中黑色固体变红 | (2)电极a附近溶液出现浑浊 | (3)中溶液出现浑浊 | (4)中溶液红色褪去 |
下列对实验现象解释不正确的是( )
A.(1)中:CuO+H2![]() Cu+H2O
Cu+H2O
B.(2)中a电极:2H2O+2e-=H2↑+2OH-,Mg2++2OH-=Mg(OH)2↓
C.(3)中:Cl2+S2-=S↓+2Cl-
D.(4)中:Cl2+H2O![]() HCl + HClO
HCl + HClO
